

分析 铬铁矿加入纯碱,通入空气煅烧,经浸取后得到Na2CrO4、Na2CO3,加入适量硫酸,得到混合溶液乙含有Na2Cr2O7和Na2SO4,然后结晶可得到Na2Cr2O7晶体,
(1)根据正负总化合价之和相等进行分析;
(2)类比Na2SiO3可写成Na2O•SiO2完成Fe(CrO2)2的氧化物的形式;
(3)根据影响化学反应速率的因素分析;
(4)①固体图示及题中信息可知,少量不能除尽Na2CO3等杂质,过量会生成Na2Cr3O10等副产物;
②发生了反应2CrO42-+2H+=Cr2O72-+H2O,生成了Na2Cr2O7和Na2SO4;
(5)a连接电源负极,所以a为阴极;b连接电源正极,所以b为电解槽的阳极;阳极发生氧化反应,阴极发生还原反应.
解答 解:(1)Fe(CrO2)2中,氧元素的化合价是-2价,总的负价是-8价,铬元素的化合价是+3价,2个铬原子化合价是+6价,所以铁元素化合价是+2价,
故答案为:+2;
(2)Fe(CrO2)2 中铁元素化合价是+2价,氧化物为FeO,铬元素化合价+3价,氧化物为Cr2O3,所以Fe(CrO2)2写成氧化物形式为FeO•Cr2O3,
故答案为:FeO•Cr2O3 ;
(3)增大反应物接触面积可以加快反应速率,升高温度可以大大加快反应速率,
故答案为:粉碎矿石、升高温度;
(4)①由于少量难以除尽碳酸钠,过量会发生反应3CrO42-+4H+=Cr3O102-+2H2O,生成了Na2Cr3O10等副产物,所以必须加入适量硫酸,
故答案为:少量不能除尽Na2CO3等杂质,过量会生成Na2Cr3O10等副产物;
②由于发生了反应2CrO42-+2H+=Cr2O72-+H2O,生成了Na2Cr2O7和Na2SO4,所以乙中溶质的化学式Na2Cr2O7和Na2SO4,
故答案为:Na2Cr2O7和Na2SO4;
(5)根据电解槽图示可知,a为阴极,溶液显示酸性,溶液中氢离子得到电子,发生还原反应,电极反应为:2H++2e-=H2↑,
b为阳极,铁失去电子生成亚铁离子,亚铁离子被Cr2O72-氧化成铁离子,反应的方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:2H++2e-=H2↑;Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
点评 本题考查了重铬酸钠的制取原理及除杂方法,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,注意合理分析题中信息,难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56gFe与足量的盐酸反应,转移的电子数为2NA | |
| B. | 标准状况下,22.4L的水中含有的原子数为3NA | |
| C. | 物质的量浓度为2mol/L的BaCl2溶液中,含有Cl-个数为4NA | |
| D. | 22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| B. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 | |
| C. | 用溶解、过滤的方法分离K2MnO4和MnO2固体的混合物 | |
| D. | 用分液的方法分离煤油和汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
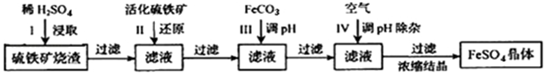
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
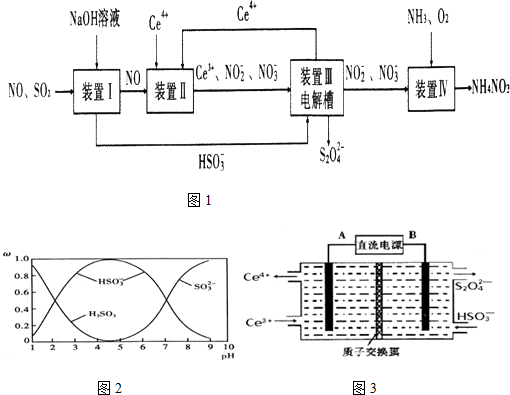
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  由如图知,石墨转变为金刚石是放热反应 | |
| B. |  由如图知,S(g)+O2(g)═SO2(g)△H1,S(s)+O2(g)═SO2(g)△H2则△H1<△H2 | |
| C. |  由如图知,白磷比红磷稳定 | |
| D. |  如由图知,CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
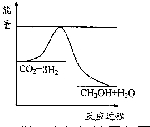 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.| 起始 浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com