
| A�� | ֻ���ݷ�ӦNH3��g��+HCl��g���TNH4Cl��s���ڵ��������Է����У������жϳ��÷�Ӧ��H������ | |
| B�� | ���ڷ�ӦN2��g��+3H2��g��$?_{����}^{���¡���ѹ}$2NH3��g�����������Ĵ�����ʹƽ��������Ӧ�����ƶ� | |
| C�� | ��ˮ�м���������ʹˮ�ĵ���ƽ�������ƶ�����ˮ�����ӻ����� | |
| D�� | �ö��Ե缫���1 L 1 mol/L��CuSO4��Һ������������3.2 gͭʱ������0.05 mol Cu��OH��2����ɽ���Һ�ָ���ԭŨ�� |
���� A������G=��H-T•��S��0ʱ����Ӧ���Է����У�
B������ֻӰ�췴Ӧ���ʣ���Ӱ�컯ѧƽ�⣻
C��ˮ�����ӻ�ֻ���¶ȵ�Ӱ�죬�¶Ȳ��䣬��ˮ�����ӻ����䣻
D��ȷ�����ʱ��Һ�����������ʣ�������ʲô��ʲô�ټ�����Ӧ������ʹ��Һ�ָ���ԭ��״̬��
��� �⣺A����Ӧ��ӦNH3��g��+HCl��g���TNH4Cl��s�����ر��S��0���÷�Ӧ�ڵ��������Է����У�˵�������¡�G=��H-T•��S��0�����H��0����A����
B���������Ĵ�������Ӱ�췴Ӧ���ʣ�����Ӱ�컯ѧƽ�⣬��ʹƽ��������Ӧ�����ƶ�����B����
C����ˮ�м������ᣬHCl�������������������ˮ�ĵ��룬ʹˮ�ĵ���ƽ�������ƶ��������¶Ȳ��䣬��ˮ�����ӻ����䣬��C��ȷ��
D�����CuSO4��Һʱ��������ͭ���ӵõ�������ͭ��������ʧ��������������������Һ�������������൱������ͭ��Ҫʹ��Һ�ָ���ԭ��״̬��������Һ�м���0.05 molCuO����Cu��OH��2�൱������ͭ��ˮ������0.05 mol��Cu��OH��2���壬����ҺƫС����D����
��ѡC��
���� ���⿼���Ϊ�ۺϣ��漰��Ӧ�����ʱ��Ӧ�á����ԭ������ѧƽ�⼰��Ӱ�졢ˮ�ĵ��뼰��Ӱ���֪ʶ����ȷ��Ӧ�Է����е�����Ϊ���ؼ���ע�����յ��ԭ������ѧƽ���Ӱ�����أ�����������ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
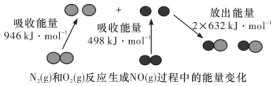 ��ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ģ���ͼΪN2��g����O2��g����Ӧ����NO��g�������е������仯������˵������ȷ���ǣ�������
��ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ģ���ͼΪN2��g����O2��g����Ӧ����NO��g�������е������仯������˵������ȷ���ǣ�������| A�� | 1 mol N2��g����1 mol O2��g����Ӧ�ų�������Ϊ180 kJ | |
| B�� | 1 mol N2��g����1 mol O2��g�������������2 mol NO��g����������� | |
| C�� | ��1 L�������з�����Ӧ��10 min�� N2 ������1 mol�����10 min�ڵ�ƽ����Ӧ����Ϊv��NO��=0.1 mol/��L•min�� | |
| D�� | NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O | B�� | CaCl2 | C�� | KOH | D�� | Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
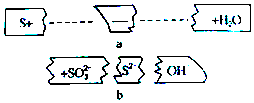
| A�� | �������뻹ԭ�������ʵ���֮��Ϊ2��1 | |
| B�� | �÷�Ӧ���������������½��� | |
| C�� | ��Ӧ������S��SO32-��OH- | |
| D�� | .2molS�μӷ�Ӧʱ��ת�Ƶĵ�����Ϊ$\frac{8}{3}$ NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
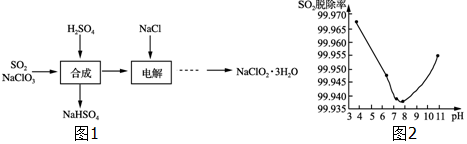
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
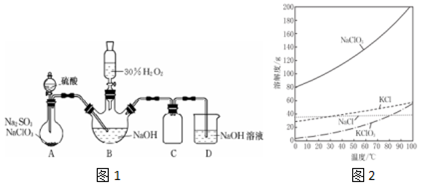
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | CO��g�� | H2��g�� | CH3OH��l�� | CH4��g�� |
| ��H/��kJ/mol�� | -283.0 | -285.8 | -726.5 | -890.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ���ϵ����� | ����� |
| ��1 | ����� | |
| ��2 | �ǵ���� | |
| ��3 | ǿ����� | |
| ��4 | ������� | |
| ��5 | �Ȳ��ǵ����Ҳ���ǵ���� | |
| 6 | �ܵ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com