
【题目】下列实验设计方案错误的是
A. 除去CO2气体中混有的HCl:饱和碳酸氢钠溶液
B. 分离碘和CCl4的混合物:分液
C. 区分NaCl和KCl溶液:焰色反应
D. 检验某未知溶液中的SO42-:加入稀硝酸酸化的BaCl2溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】2015年,中国科学家屠呦呦获得了诺贝尔医学奖,因为发现青蒿素,一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命.
如图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
A.青蒿素分子式为C15H22O5
B.青蒿素易溶于乙醇、苯
C.青蒿素因含有﹣O﹣(醚键)而具有较强的氧化性
D.青蒿素在碱性条件下易发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的NaHCO3和Na2O2混合物置于一密闭容器中充分加热,反应物中转移电子的物质的量为1mol,下列说法一定正确的是( )
A.混合物中NaHCO3和Na2O2物质的量一定相等
B.容器中肯定有0.5molO2
C.反应后容器中的固体只有Na2CO3
D.反应后容器中一定没有H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体X是由两种常见元素组成的化合物,其中金属元素与另一元素的质量比为14:1。在一定条件下X可发生如图的转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为气体混合物,R是一种无色无味能使澄清石灰水变浑浊的气体,C为红褐色沉淀,M为一种常见金属单质。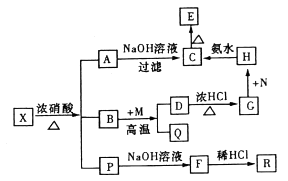
试回答下列问题:
(1)X的化学式为。
(2)实现G→H,欲不引进新的杂质,N可以选择下列物质中的(填序号)。
①KMnO4 ②HNO3 ③H2O2 ④Cl2
(3)写出下列转化的化学方程式:
B→D:;H→C:。
(4)已知P中有一种气体与氢氧化钠溶液反应可生成两种正盐,该反应的离子方程式为:。
(5)X与浓硝酸在一定条件下反应时,若有1 mol X被氧化时,转移的电子数目为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、C原子都有两个未成对的单电子,D的二价阳离子与C的阴离子具有相同的电子层结构. B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 .
(2)B的氢化物的分子空间构型是 , 其中心原子的杂化方式是 .
(3)AC2的电子式 , 是分子(填“极性”或“非极性”),一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(4)E的核外电子排布式是 , ECl3与B、C的氢化物形成的配合物的化学式为 .
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中横行的编排依据是( )
A. 按元素的相对原子质量递增顺序从左到右排列
B. 按元素的原子核外电子层数依次递增顺序从左到右排列
C. 电子层相同的元素,按原子序数依次递增顺序从左到右排列
D. 按元素的原子最外层电子数依次递增顺序从左到右排列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜的制备实验是化学实验教学中一个必做实验,某学习小组设计了如下两个实验方案:
(1)实验一:
因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
根据上述实验和反应,比较浓硫酸与稀硫酸的性质,浓硫酸具有。
(2)该反应的化学方程式为。
(3)实验二:
以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,其反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
Fe2(SO4)3的作用是。
(4)得到的混合液可以用下列四种物质中的调节溶液的pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH
B.CuO
C. CuCO3
D.Fe
(5)请根据以上内容,对这两个实验方案进行评价,填下表:
实 验 (一) | 实 验 (二) | |
主要优点 | 操作简便 | ⑴原料充分转化为产品 |
主要缺点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )
A.1个乙分子中含有2个A原子
B.摩尔质量关系为:2M (甲)=M (乙)+M (丙)
C.该反应一定属于氧化还原反应
D.该反应类型是分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com