
| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-甲基-3-乙基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
分析 烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析.
解答 解:A、此烷烃在主链上有4个碳原子,在2号和2号碳原子上各有一个甲基,故名称为:2,3-二甲基丁烷,故A正确;
B、烷烃命名时,要选最长的碳链为主链,故主链上有4个碳原子,从离支链近的一端给主链上碳原子编号,故在2号碳原子上有2个甲基,故名称为:2,2-二甲基丁烷,故B错误;
C、烷烃命名时,要选最长的碳链为主链,故此烷烃中主链上有5个碳原子,从离支链近的一端给主链上碳原子编号,当两端离支链一样近时,要从支链多的一端开始编号,当两端支链一样多是,要从支链简单的一端开始编号,故在2号碳原子上有一个甲基,在3号碳原子上有一个乙基,故名称为:2-甲基-3-乙基戊烷,故C正确;
D、烷烃命名时,要选最长的碳链为主链,故在主链上有4个碳原子,从离支链近的一端给主链上碳原子编号,而两端离支链一样近,且支链一样多,故在2号碳原子、3号碳原子上各有两个甲基,故名称为:2,2,3,3-四甲基丁烷,故D正确.
故选B.
点评 本题考查了烷烃的命名,应注意的是烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,掌握烷烃的命名规则是解题关键.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:解答题
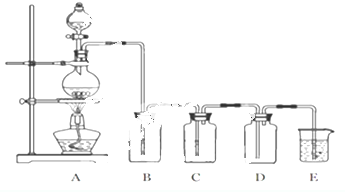
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
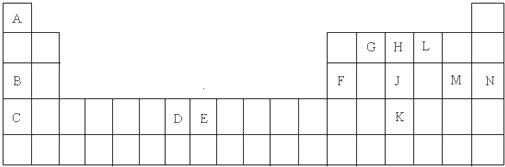
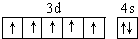 ,在其化合物中,最高正价是+7;
,在其化合物中,最高正价是+7;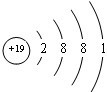 ;
;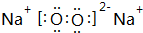 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
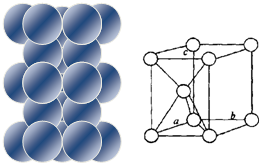 | (1)镁原子在二维空间的配位数为6 (2)位于晶胞中部的镁原子与离它最近两平面相切(填“相离”或“相切”或”相交”) |
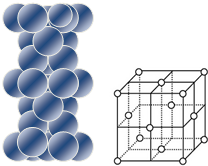 | (3)铜原子在三维空间的配位数为12 (4)请用含R2、NA的数学式子表达金属铜的密度:$\frac{8\sqrt{2}}{{N}_{A}•{{R}_{2}}^{3}}$g/cm3(根号带在分子上) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-二甲基-3-乙基丁烷 | B. | 2,2,3-三甲基戊烷 | ||
| C. | 2,2-二甲基-3-乙基丁烷 | D. | 3,4,4-三甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气具有还原性,可用作制冷剂 | |
| B. | NaHCO3能与碱反应,可用作焙制糕点的膨松剂 | |
| C. | 小苏打可与酸反应,可用作治疗胃酸过多的药剂 | |
| D. | 碳酸钠溶液显碱性,可用作锅炉除垢时CaSO4沉淀的转化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅥA | ⅦA | O | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com