
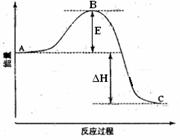
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
(1)图中A表示 ,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”),理由是
(2)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求计算过程)。
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
下列说法错误的是 ( )
A.钠和铁一样,都能在氯气中燃烧生成金属氯化物
B.液氯是氯气的水溶液,它能使干燥的有色布条褪色
C.氯气跟变价金属反应生成高价金属氯化物
D.氯水具有杀菌、漂白作用是因为氯水中含有强氧化性的次氯酸
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下图中物质M是由同一短周期的两种元素组成的离子化合物,焰色反应为黄色,阴离子元素最高正价与它的负价代数和为6。X具有漂白性,Y为碱性气体,W是对空气无污染的气体。试回答下列问题:
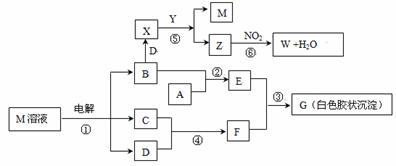
(1)写出电解M溶液①的化学方程式 。
(2)已知工业上制备Y气体,每生成1molY时放出的热量为akJ(该热量已合算成25℃,101KP),请写该反应的热化学方程式 。
(3)若A是一种常见金属,写出反应②的离子方程式 。
(4)若A是某元素的一种常见酸性氧化物,则A的化学式为 ;其用途为 。(写出一种即可)
(5)写出反应⑤的化学方程式 。
(6)标准状况下,反应⑥中生成11.2L W时转移的电子数 。(用NA表示阿伏加德罗常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗的NaOH的物质的量( )
| A. | 中和CH3COOH的多 | B. | 中和HCl的多 |
| C. | 相同 | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:( )
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:( )
A.用物质A表示的反应平均速率为0.3 mol·L-1·s-1
B.用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
C.2 s时物质A的转化率为70%
D.2 s时物质B的浓度为0.7 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习,下列物质的分类不正确的是
A.SO2(氧化物) B.稀硫酸(电解质) C.HNO3(含氧酸) D.氯水(混合物)
查看答案和解析>>
科目:高中化学 来源: 题型:
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。右上图是
已经合成的最著名的硫-氮化合物(S4N4)的分子结构,下列关于S4N4的说法中不正确的是
A.S4N4属于共价化合物 B.S4N4中硫元素与氮元素的质量比为1:1
C.S4N4分子中既有极性键又有非极性键 D.S4N4分子中所有原子的最外层都达到8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体单质,各物质有以下的转化关系(部分产物及条件略去),回答问题:
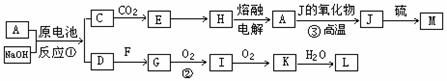
(1)写出该原电池的总反应方程式 。
(2)写出②的化学方程式 。
(3)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为 。(写出计算式)
(4)若③中J的氧化物为磁性氧化物,且每生成1mol J放出QkJ的热量,请写出A→J反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学—选修:化学与技术]
SO2、NO是大气污染物。吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
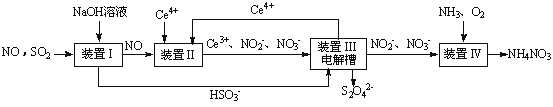
 (1)装置Ⅰ中生成HSO3-的离子方程为 。
(1)装置Ⅰ中生成HSO3-的离子方程为 。
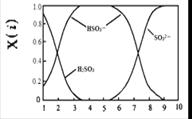
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如右图所示。
①下列说法正确的是 (填字母序号)。
a.pH=8时,溶液中c(HSO3-) < c(SO32-)
b.pH=7时,溶液中c(Na+) =c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
 (3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 。
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 。
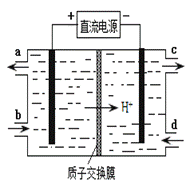
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
①生成Ce4+的电极反应式为 。
②生成Ce4+从电解槽的 (填字母序号)口流出。
已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com