
| A. | Na和Cl | B. | K和F | C. | H和Cl | D. | Ca和O |
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 达到平衡时,SO2的浓度与SO3的浓度相等 | |
| B. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| C. | 为了提高SO2的转化率,应适当提高O2的浓度 | |
| D. | 在上述条件下,SO2不可能100%转化为SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z、N的简单离子的还原性:Z2->N- | |
| B. | Y2X和Y2X2都是碱性氧化物 | |
| C. | Z与X形成的化合物对应的水化物一定是强酸 | |
| D. | Z元素的非金属性比N元素的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28% | B. | 27.6% | C. | 72.4% | D. | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=0.33 kJ•mol-1 | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | 正交硫比单斜硫稳定 | |
| D. | 单斜硫比正交硫稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它属于有机高分子 | B. | 它能产生“白色污染” | ||
| C. | 它形成的单体是乙烯 | D. | 聚乙烯中含有双键不稳定,易变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
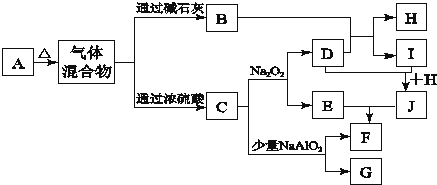
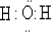 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
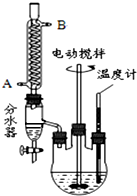 最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如图:
最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如图: +C4H9OH$\stackrel{H_{2}SO_{4}}{→}$
+C4H9OH$\stackrel{H_{2}SO_{4}}{→}$ 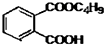 $→_{C_{4}H_{9}OH}^{H_{2}SO_{4}}$
$→_{C_{4}H_{9}OH}^{H_{2}SO_{4}}$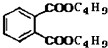
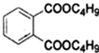 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$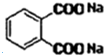 +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com