
| A. | 金属元素与非金属元素形成的化学键一定是离子键 | |
| B. | ⅠA族和ⅦA族原子化合时,一定生成离子键 | |
| C. | 仅非金属元素形成的化合物中一定不是离子键 | |
| D. | 活泼金属与活泼非金属化合时,能形成离子键 |
分析 A.金属元素和非金属元素之间可能形成共价键;
B.第IA族和第VIIA族元素之间可能形成共价键;
C.仅含有非金属元素的化合物中可能含有离子键;
D.活泼金属和活泼非金属元素之间易形成离子键.
解答 解:A.金属元素和非金属元素之间可能形成共价键,如氯化铝,故A错误;
B.第IA族和第VIIA族元素之间可能形成共价键,如HX,故B错误;
C.仅含有非金属元素的化合物中可能含有离子键,如铵盐,故C错误;
D.活泼金属和活泼非金属元素之间易形成离子键,原子之间通过得失电子形成离子键,故D正确;
故选D.
点评 本题考查离子键判断,为高频考点,明确物质构成微粒及微粒之间作用力是解本题关键,易错选项是C,注意规律中的反常现象,如BC.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子核外各电子层上的电子数均已达到2n2 | |
| B. | 所有电子在同一区域里运动 | |
| C. | 能量高的电子在离核近的区域运动 | |
| D. | 能量低的电子在离核近的区域绕核运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 碳元素能够形成不同的单质,如C60、C70、金刚石等等.
碳元素能够形成不同的单质,如C60、C70、金刚石等等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M元素一定是第VA族元素 | |
| B. | M元素一定是第三周期元素 | |
| C. | M可形成与CH3CHO电子数相等的化合物 | |
| D. | M的单质在空气中加热时可能会生成红棕色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
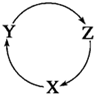 下列各组物质中,满足下图物质一步转化关系的选项是( )
下列各组物质中,满足下图物质一步转化关系的选项是( )| X | Y | Z | |
| A | Fe | FeCl3 | FeCl2 |
| B | NH3 | NO | NO2 |
| C | Na | NaOH | Na2CO3 |
| D | S | SO3 | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$mol/(L•min) | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 三个容器中反应的平衡常数均为K=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| W | X | Y | |
| Z |
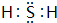 .
.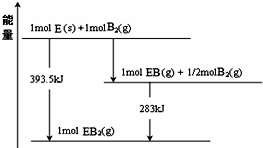
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI═Z↓+2I2+3H2O |
| ① | 还原性 | |
| ② | H2ZO3+2NaOH═Na2ZO3+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com