
����Ŀ��̼Ԫ������Ȼ�����Զ�����̬���ڡ�
I����ͼA��B�ֱ��ʾ���ʯ��ʯī�Ľṹģ�͡��ұ�Ϊ���ʯ��ʯī��ijЩ���ʣ�
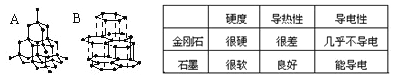
��1�����ʯת��Ϊʯī����_________�仯�����������ѧ������
��2���и���IJ�����Ӧѡ��________________������ʯ����ʯī���������ϡ�
��3�����ݽ��ʯ��ʯī�Ľṹ�������ƶϣ������۵�����ȷ����___������ĸ��
A����ͬ���ʾ��в�ͬ�Ľṹ B����ͬ���ʵ����Ԫ��һ����ͬ
C����ͬ���ʾ��в�ͬ������ D�����ʵĽṹ���������ʵ�����
II��̼������̼����Ҫ�����̼���ƺ�̼��������Ӧ�ù㷺������̼���Ρ�
��4��̼���������ճ������е�һ����;��____________________��
��5������һ����ɫ���壬Ϊ����÷�ĩ��̼���ƻ���̼�����ƣ�ijͬѧ������·�����չʵ�顣�����Ҫ����д�հף�
ʵ����� | �йط�Ӧ�Ļ�ѧ����ʽ | ʵ����� |
ȡ������ĩ�����Թ��м��ȣ���������������ͨ�����ʯ��ˮ�� | ______________________________________________________________________________ | �÷�ĩΪ ̼������ |
���𰸡� ��ѧ ���ʯ B ���Ʒ��ͷ� 2NaHCO3=Na2CO3+H2O+CO2�� CO2+Ca(OH)2=CaCO3��+H20
����������1�����ʯ��ʯī�������ֲ�ͬ������������ת��Ϊ��ѧ�仯��
��2�����ݽ��ʯӲ�ȴ���з�����
��3���������ʵ���ɡ��ṹ�����ʵȽ��з�����
��4��̼���������ճ����������Ʒ��ͷ۵���
��5��̼�������Ȳ��ֽ⣬̼�����������ֽ�����Ӧ����������ͨ������ʯ��ˮ������Һ�������
��1�����ʯ��ʯī�������ֲ�ͬ�����������Խ��ʯ��ΪʯīΪ��ѧ�仯����ȷ������ѧ��
��2�����ʯӲ�Ƚϴ��������������и���IJ���������ȷ�������ʯ��
��3����ͬ���ʾ��в�ͬ�Ľṹ��A��ȷ����ͬ���ʵ����Ԫ�ز�һ����ͬ�����������ʯ��ʯī�Dz�ͬ������,���Ԫ����ͬ��B��������ͬ���ʾ��в�ͬ������,C��ȷ�����ʵĽṹ���������ʵ�������D��ȷ����ȷѡ��B��
��4��̼��������Һ�Լ��ԣ��ܹ��к���������ճ������г��������Ʒ��ͷ۵�����ȷ�������Ʒ��ͷ���
��5��̼�������Ȳ��ֽ⣬̼�����������ֽ⣬����ʽΪ2NaHCO3=Na2CO3+H2O+CO2������Ӧ����������ͨ������ʯ��ˮ������Һ���������Ӧ�ķ���ʽ��CO2+Ca(OH)2=CaCO3��+H20����ȷ�𰸣�2NaHCO3=Na2CO3+H2O+CO2����CO2+Ca(OH)2=CaCO3��+H2O��


 С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(I)ʵ���Һϳ����������IJ��裺��Բ����ƿ�ڼ����Ҵ���Ũ��������ᣬƿ����ֱ��װͨ����ȴˮ��������(ʹ��Ӧ��������������ΪҺ��������ƿ�ڣ������Ȼ���һ��ʱ�������װ�ý������õ������Ҵ��������ˮ�����������ֲ�Ʒ����ش��������⣺
��1������ƿ�г��˼����Ҵ���Ũ�����������,��Ӧ��____ ��Ŀ����_______��
��2����Ӧ�м�������Ҵ���Ŀ���� _______��
(��)��֪��ϩ�ܷ�������ת����
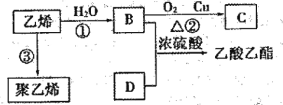
��1��д�����л�������������ƣ�B�к�����������__________��D�к����������� _____ ��
��2��д����Ӧ�Ļ�ѧ����ʽ��
��__________��
��__________��
��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ�־��в���������ʳ�����ϣ��ǻ�������뱽������ ![]() ����������Ӧ�IJ��
����������Ӧ�IJ��
��1����һ�����еĹ����ŵ������� ��
��2��5.8g����ȫȼ�տɲ���0.3mol CO2��0.3mol H2O��������������������ܶ���29�������в���������Ϊ��״�ṹ����ṹ��ʽ�ǣ� ��
��3�����������ж��������ͬ���칹�壬��������FeCl3��Һ������ɫ��Ӧ������2��һ����ȡ�����ͬ���칹���ǣ���д2�ֽṹ��ʽ���� ��
��4����֪��R��CH2��COOH ![]()
![]() R��ONa
R��ONa ![]() R��O��R�䣨R����R�䩁���������� �������ĺϳ�·�����£�
R��O��R�䣨R����R�䩁���������� �������ĺϳ�·�����£�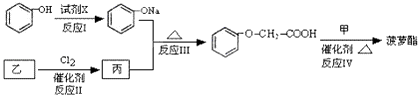
���Լ�X����ѡ�õ��ǣ�ѡ����ĸ�� ��
a��CH3COONa��Һ���� b��NaOH��Һ
c��NaHCO3��Һ���� d��Na
�ڱ��Ľṹ��ʽ�� �� ��Ӧ��ķ�Ӧ������ ��
�۷�Ӧ���Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ͼ���Ƽ��仯����ת���������У�����ȷ���� �� ��

A. ��Ϊ���Ϸ�Ӧ B. ��Ϊ�û���Ӧ
C. ��������ԭ��Ӧ D. ��Ϊ��������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��C��O��Si��S��Fe����Ҫ�Ļ�ѧԪ�أ�����ѧ��ѧ�ж����ǵĵ��ʺͻ�������о��Ķࡣ
��1��C��O��Si����Ԫ�ص�һ�������ɴ�С��˳����_______________________��
��2��CS2����Ҫ���ܼ���CS2��Cԭ�ӵ��ӻ���ʽΪ_____________����ռ乹��Ϊ_______________��
��3����̬Feԭ���У��������ռ������ܲ�ķ�����________��ռ�ݸ��ܲ���ӵĵ���������ͼ��״Ϊ_______________��
��4�������Ƶ��������������⾧��ṹ��
����NaC1����������ͼ���е�����C1-ȥ��������Na+ȫ������Siԭ�ӣ����ڼ������С�����������Ĵ�������һ��Siԭ�ӱ㹹���˾���Si��һ��������������ÿ�������������Siԭ���������ߵ��е㴦����һ��Oԭ�ӣ��㹹����SiO2�������ɴ˿�����SiO2��������______��Siԭ�ӣ�______��Oԭ�ӡ�
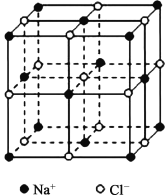
����������NaC1�����Ƶ���CsC1�����ķ�����____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�мס���ֱ�Ϊ�������������е�һ�֣�CuSO4��H2SO4��Fe��Na2CO3��Ca(OH)2����ͼ��������������Ӧ�����ʣ�������Һ���ڳ����������ܷ�����ѧ��Ӧ��

��1����������������
�ٿ�����ũҵ��������������������_________________��
����������û���Ӧ��һ����ѧ����ʽΪ_________________________��
��2����ͼ����ΪH2SO4��
�ټ���ܷ�ΪCuSO4����_____________������ԡ������ԡ�����
�������붡�����кͷ�Ӧ�����Ϊ_________________��
��3������Ϊ����������췴Ӧ�����ӷ���ʽΪ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����22.4g�������뵽��HNO3 0.8mol��ϡ�����У���Ӧ���ɵ���������ʵ�����x�����������۵����ʵ�����y���仯��ϵ����ȷ���ǣ�������
A.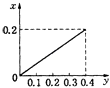
B.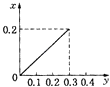
C.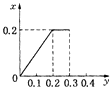
D.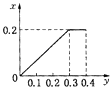
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ����pH��2��ǿ����Һ��pH��13��ǿ����Һ��ϣ����û��Һ��pH��11����ǿ����Һ��ǿ����Һ���������(���Ի�Ϻ���Һ������仯)
A. 11��1 B. 9��1 C. 1��11 D. 1��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
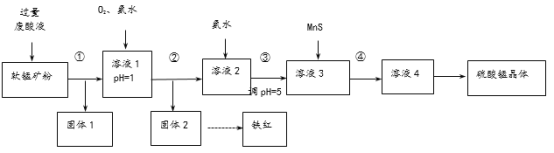
����Ŀ�������̿�����Ҫ�ɷ�MnO2������Fe2O3��Cu2(OH)2CO3������������ˮ���������������ϴ������Һ����1mol/LH2SO4��FeSO4��Һ���������������̺�������Fe2O3����������������ͼ��
Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 | |
��ʼ����ʱ | 8.3 | 6.3 | 4.7 | 2.7 |
��ȫ����ʱ | 9.8 | 8.3 | 6.7 | 3.6 |
��1��������~�����漰��ʵ����������У��������˵���______��д�������
��2����Һ1�У���ͨ��O2����������_______��
��3���ɹ���2�õ�����Ļ�ѧ����ʽ��_______��
��4������˵����ȷ����______������ĸ����
a�����̢�����������ԭ��Ӧ����
b������MnS��Ŀ���dz�ȥ��Һ�е�Cu2+������Mn2+
c����Һ1�к��е���������Ҫ��Fe2+��Fe3+��Cu2+��Mn2+��H+
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com