

| A. | 装置①中SO42-的向Al片移动 | |
| B. | 装置②中的Mg片上发生的反应为:2H++2e-═H2↑ | |
| C. | 装置③中铁片被氧化,铜片上产生气体 | |
| D. | 装置④中若有1摩尔铁锈(氧化铁)生成,理论上有4摩尔电子通过导线 |
分析 A、装置①中铝比镁活泼为负极,阴离子移向负极;
B、原电池的正极发生得电子的还原反应;
C、金属铁在常温下遇浓硝酸钝化;
D、铁、铜、氯化钠构成的原电池中,金属铁发生的是吸氧腐蚀.
解答 解:A、装置①中铝比镁活泼为负极,阴离子移向负极,所以SO42-的向Al片移动,故A正确;
B、②中的氧化还原反应发生在金属铝和氢氧化钠之间,失电子的是金属铝,为负极,Mg作为正极,电极反应式为6H2O+6e-═6OH-+3H2↑,故B错误;
C、金属铁在常温下遇浓硝酸钝化,铁为正极,铜为负极,所以装置③中铜片被氧化,铁片上产生气体,故C错误;
D、铁、铜、氯化钠构成的原电池中,金属铁为负极,金属铜为正极,铁发生的是吸氧腐蚀,若有1摩尔铁锈(氧化铁)生成,理论上有6摩尔电子通过导线,故D错误.
故选A.
点评 本题考查学生原电池的工作原理知识,可以根据所学内容来回答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上层倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 配浓硫酸和浓硝酸的混酸时,应将浓硫酸慢慢加到浓硝酸中,及时搅拌和冷却 | |
| D. | 测溶液的pH值需先用蒸馏水润湿pH试纸,再用干燥洁净的玻璃棒蘸溶液滴在试纸上,并与标准比色卡对照 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
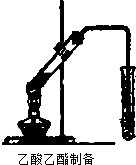 某校化学兴趣学习小组实验探究乙醇的性质.
某校化学兴趣学习小组实验探究乙醇的性质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 加入试剂 | 操作方法 |
| ①苯(苯甲酸) | (2) | (4) |
| ②蛋白质(NaCl) | (3) | (2) |
| ③肥皂(甘油) | (1) | (7) |
| ④乙醇(水) | (4) | (3) |
| ⑤乙酸乙酯(乙酸) | (5) | (4) |
| ⑥乙烷(乙烯) | (6) | (6) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氰分子中四原子共直线 | |
| B. | 氰分子中C≡N键长大于C≡C键长 | |
| C. | 氰气分子中含有σ键和π键 | |
| D. | 氰化氢在一定条件下能与烯烃发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3+HNO3;Na2CO3+HCl | B. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | ||
| C. | NaOH+H2SO4;KOH+NaHSO4 | D. | Na2CO3+HCl(少量);Na2CO3(少量)+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和NaHSO3溶液 | B. | 饱和Na2CO3溶液 | C. | 饱和NaHCO3溶液 | D. | 固体CaO粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 表述I | 表述II |
| A | SiO2有导电性 | SiO2可用于制备光导纤维 |
| B | SO2有漂白性 | SO2可使溴水褪色 |
| C | 溶液中含有大量的NO3- | 溶液中不能存在大量I-或S2- |
| D | 将淀粉与KCl混合液装于半透膜内,浸泡在盛蒸馏水的烧杯中,5min后取烧杯中液体,加碘水变蓝色 | 半透膜有破损 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com