
| A. | 该反应中的氧化剂只有Cu2O | |
| B. | Cu2O在反应中既是氧化剂又是还原剂 | |
| C. | Cu既是氧化产物又是还原产物 | |
| D. | 氧化产物与还原产物的物质的量之比为1:6 |
分析 Cu2S+2Cu2O $\frac{\underline{\;\;△\;\;}}{\;}$ 6Cu+SO2↑中,Cu元素的化合价降低,S元素的化合价升高,以此来解答.
解答 解:A.Cu元素的化合价降低,则Cu2O、Cu2S均为氧化剂,故A错误;
B.Cu元素的化合价降低,S元素的化合价升高,则Cu2S在反应中既是氧化剂,又是还原剂,Cu2O在反应中仅是氧化剂,故B错误;
C.Cu元素得到电子被还原,则Cu为还原产物,故C错误;
D.Cu为还原产物,SO2为氧化产物,由反应可知,氧化产物与还原产物的物质的量之比为1:6,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 形成化学键时吸收能量 | |
| B. | 中和反应是吸热反应 | |
| C. | 燃烧属于放热反应 | |
| D. | 反应物总能量与生成物总能量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L的Na 2A溶液中:c(A 2-)+c(HA -)+c(H 2A)=0.1mol/L | |
| B. | 常温下,将pH=3的H 2A溶液稀释到原来的100倍,则稀释后溶液的pH<5 | |
| C. | 常温下,将pH=3的H 2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性 | |
| D. | 常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na +)-c(HA -)-c(A 2-)=10 -5-10 -9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 将碘水和四氯化碳的混合溶液置于分液漏斗中并振荡、静置.溶液分层,上层呈紫红色,下层几乎无色. | 碘在四氯化碳中的溶解度大于在水中的溶解度 |
| B | 将表面滴有几滴水的蔗糖和一定量的浓硫酸混合并搅拌.蔗糖膨胀变黑,产生有刺激性 气味的气体. | 浓硫酸具有脱水性和强氧化性 |
| C | 在稀硝酸和过量的铜片反应后的溶液中,滴入少量稀硫酸.剩余铜继续溶解,并有气泡产生. | 稀硫酸也可将铜氧化 |
| D | 用洁净的铂丝蘸取某盐溶液在酒精灯火焰上灼烧.观察到酒精灯火焰呈黄色. | 盐溶液中一定含有 Na+,无 K+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水库的钢闸门接直流电源的正极,可以减缓闸门的腐蚀 | |
| B. | 加入少量硫酸铜可加快锌与稀硫酸的反应速率,说明Cu2+具有催化作用 | |
| C. | H2O2分解产生标准状况下22.4 L O2,理论上转移电子数约为4×6.02×1023 | |
| D. | 常温下pH=3的盐酸与pH=11的某碱溶液等体积混合,若溶液呈碱性,该碱为弱碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液漏斗使用前需要先检查是否漏液 | |
| B. | 试验中剩余的钠不能再放回原试剂瓶 | |
| C. | 做焰色反应时,铂丝应用盐酸洗净并灼烧至无色 | |
| D. | 蒸馏烧瓶加热时需要垫石棉网 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
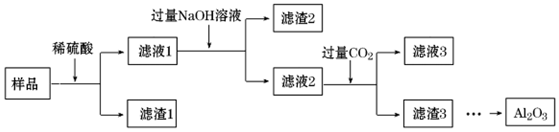
| A. | 滤渣1 的主要成分为SiO2 | |
| B. | 可用KSCN溶液检验滤液1中的Fe 3+ | |
| C. | 滤液2为纯净的Na AlO2溶液 | |
| D. | 将滤渣3 洗涤、干燥、灼烧,可以得到Al2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com