
 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.| △c |
| △t |
| △c |
| △t |
| ||
| 5min |


科目:高中化学 来源: 题型:
| A、着色剂--胡萝卜素、苯甲酸钠 |
| B、调味剂--亚硝酸钠、味精 |
| C、防腐剂--氯化钠、柠檬黄 |
| D、营养强化剂--酱油中加铁、粮食制品中加赖氨酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(B) |
| c(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Cu2O/ZnO |
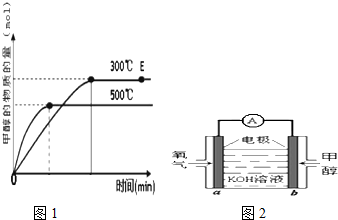
| 1 |
| 2 |
| c(CH3OH) |
| c(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)/mol.L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| C(CO)/mol.L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
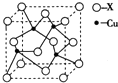 (1)HCNO是一种弱酸,它的酸性类似于醋酸,在水中微弱地电离出H+和CNO-.
(1)HCNO是一种弱酸,它的酸性类似于醋酸,在水中微弱地电离出H+和CNO-.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com