【化学与技术】
请回答氯碱工业的有关问题:
(1)以前采用无隔膜电解冷的食盐水时,Cl
2会与NaOH接触,产物中肯定有NaClO,从而影响产品的纯度,能包含这一过程的总化学方程式为
;所以现代氯碱工业多采用隔膜法进行电解,即用隔膜将电解槽分隔成阳极区和阴极区,则从阴极区排出的是
.
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上.在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.
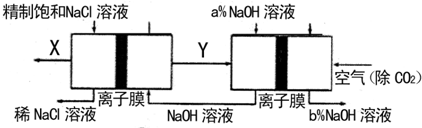
分析比较图示中氢氧化钠质量分数a%与b%的大小:a%
b%(填>,=或<),
理由是:
.
(3)科研人员为减少火力发电厂对环境的污染,曾经考虑让火力发电厂和氯碱制造厂进行就近联合.请你判断该方案是否可行?
;理由是
:
A.发电厂的废气(SO
2)与氯碱厂的Cl
2或NaOH反应,减少了SO
2的排放
B.可产生多种化学原料
C.就近联合还能减少电力输送中的损耗
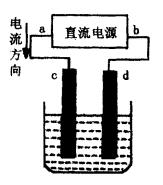
(4)将酸碱中和反应作为电池反应,可以设计出相应的电池.现将两个氢电极(以Pt 作为导电的惰性金属,以氢气作为参与电极反应的物质,可以是生成氢气,也可以是消耗氢气)分别置于酸性水溶液( H
+)和碱性水溶液(OH
-)中构成电池,使电池反应为酸碱中和反应.
①酸溶液中的氢电极A 和碱溶液中的氢电极B,为电池正极是
(填A 或B);
②B极上发生的电极反应为:
.

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案


 Ⅰ
Ⅰ
