
 X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气态单质.回答下列问题(相关回答均用元素符号表示):
X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气态单质.回答下列问题(相关回答均用元素符号表示):分析 X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大,R的基态原子在前四周期元素的基态原子中单电子数最多,所以R的核外电子排布式为1s22s22p63s23p63d54s1,为24号铬元素,x2-和Y+有相同的核外电子排布,所以X和Y分别位于第ⅥA族和ⅠA族,且X在Y的上一周期,所以XY分别为氧和钠,或硫和钾,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气态单质,X、Y、Z的原子序数都小于24,Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低,说明Z是磷、硫、氯中的某一种,结合元素化合物知识中实验室制氯气的方法,可知,X为氧元素,W为锰元素,Z为氯元素,则Y为钠元素,据此可以答题.
解答 解:X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大,R的基态原子在前四周期元素的基态原子中单电子数最多,所以R的核外电子排布式为1s22s22p63s23p63d54s1,为24号铬元素,x2-和Y+有相同的核外电子排布,所以X和Y分别位于第ⅥA族和ⅠA族,且X在Y的上一周期,所以XY分别为氧和钠,或硫和钾,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气态单质,X、Y、Z的原子序数都小于24,Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低,说明Z是磷、硫、氯中的某一种,结合元素化合物知识中实验室制氯气的方法,可知,X为氧元素,W为锰元素,Z为氯元素,则Y为钠元素,
(1)铬是24号元素,它的基态原子的核外电子排布式是1s22s22p63s23p63d54s1,
故答案为:1s22s22p63s23p63d54s1;
(2)HF分子间能形成氢键,故其沸点比较HCl高,
故答案为:HF分子间能形成氢键,而HCl分子之间不存在氢键;
(3)根据氯和氧可以存在化合物二氧化氯且氧显-2价可知,氧元素的电负性大于氯元素,Z的某种含氧酸盐常用于实验室中X的单质的制取,此含氧酸盐为氯酸钾,此酸根为氯酸根(ClO3-),其中氯原子的价层电子对数为:$\frac{7+1}{2}$=4,孤电子对数为1,所以Cl的空间构型为三角锥形,其中氧原子和氯原子之间是共价键,根据价层电子对互斥理论,孤电子对与共用电子对的之间的斥力大于共用电子对与共用电子对之间的斥力,所以ClO3-中O-Cl-O键的键角小于109.50,
故答案为:O;三角锥形;共价键;<;
(4)图中空心球的个数为$8×\frac{1}{8}+6×\frac{1}{2}$=4,实心球的个数为8,所以空心球代表氧离子,实心球代表钠离子,根据Na2O的晶胞结构图可知,氧离子周围最近的钠离子个数为8个,以相距一个氧离子最近的所有钠离子为顶点构成的几何体为立方体,由于钠离子的半径大于镁离子,所以在氧化钠中的晶格能小于氧化镁,所以氧化镁的熔点高于氧化钠,
故答案为:8;立方体;MgO;
(5)根据均摊法可知,在每个Na2O的晶胞中含有钠离子数为8,含有氧离子数为$8×\frac{1}{8}+6×\frac{1}{2}$=4,所以一个晶胞的质量为$\frac{4×62}{N{\;}_{A}}$g,Na2O的密度为:$\frac{\frac{4×62}{N{\;}_{A}}}{(a×10{\;}^{-10}){\;}^{3}}$=$\frac{4×62}{N{\;}_{A}×a{\;}^{3}×10{\;}^{-30}}$,
故答案为:$\frac{4×62}{N{\;}_{A}×a{\;}^{3}×10{\;}^{-30}}$.
点评 本题主要考查了根据元素原子结构和元素的性质推断元素种类,并在此基础上考查核外电子排布、氢键、离子空间构型、晶格能对物质性质的影响、晶胞密度的计算,中等难度,本题的解题难点在于运用元素化合知识综合确定元素的各类.


科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 | 提纯方法 |
| A | BaSO4 | BaCO3 | 水 | 溶解、过滤、洗涤 |
| B | CO2 | SO2 | 饱和 Na2CO3 溶液 | 洗气 |
| C | 乙烷 | 乙烯 | 酸性 KMnO4 溶液 | 洗气 |
| D | 蛋白质 | 葡萄糖 | 浓 (NH4)2SO4 溶液 | 盐析、过滤、洗涤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②反应均是氧化还原反应 | |
| B. | KI在整个反应过程中起催化作用 | |
| C. | KI在整个反应过程中起氧化作用 | |
| D. | “溶液突然变为蓝色,随之又很快消失”这一现象与①②的反应速率有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 正反应速率 | 逆反应速率 | |
| A | vA=2 mol/(L•min) | vB=2 mol/(L•min) |
| B | vA=2 mol/(L•min) | vC=2 mol/(L•min) |
| C | vA=1 mol/(L•min) | vB=2 mol/(L•min) |
| D | vA=1 mol/(L•min) | vC=1.5 mol/(L•min) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3 mol•L-1的Na2SO4溶液中含有的Na+和SO42-的总物质的量为0.9 mol | |
| B. | 当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol•L-1,只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol•L-1 | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 10℃时,0.35 mol•L-1的KCl饱和溶液100 mL蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
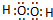 ,W第一步电离方程式为H2O2?H++HO2-.
,W第一步电离方程式为H2O2?H++HO2-.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
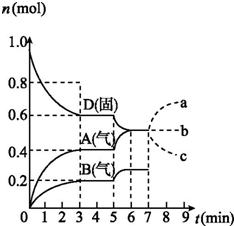 在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是( )
在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是( )| A. | 从反应开始到第一次达到平衡时,B物质的平均反应速率为0.033 3 mol/(L•min) | |
| B. | 根据右图该反应的平衡常数表达式为K=c2(A)•c(B) | |
| C. | 若在第5 min时升高温度,则该反应的正反应是吸热反应,反应的平衡常数增大,B的反应速率增大 | |
| D. | 若在第7 分钟时增加D的物质的量,A的物质的量变化情况符合a曲线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
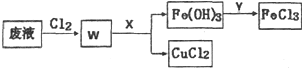 铜及其化合物在工农业生产中有着广泛的用途.
铜及其化合物在工农业生产中有着广泛的用途.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com