
分析 (1)依据玻璃棒在溶解和移液操作时作用解答;
(2)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析,凡是使物质的量n偏大,或者使溶液体积V偏小的操作都会使溶液浓度偏大,反之使溶液浓度偏低.
解答 解:(1)配制时,该实验两次用到玻璃棒,在溶解氢氧化钠固体时,用玻璃棒搅拌,加速氢氧化钠固体溶解速率;在移液时,玻璃棒起到引流作用;
故答案为:搅拌;引流;
(2)①没有洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
②定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高;
故答案为:偏高;
③容量瓶没有干燥,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不受影响;
故答案为:无影响.
点评 本题考查了一定物质的量浓度溶液的配制,熟悉配制原理和误差分析方法是解题关键,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Na+>Mg2+>Al3+ | B. | 还原性:Cl->Br->I- | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 燃料电池作为一种新型能源由于电极材料丰富,电解质多样(可以是固态、液态、气态等),将渗透到我们生活的各个领域.
燃料电池作为一种新型能源由于电极材料丰富,电解质多样(可以是固态、液态、气态等),将渗透到我们生活的各个领域.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种重要的化工原料和医药中间体,实 验室合成三苯
)是一种重要的化工原料和医药中间体,实 验室合成三苯 +H2O
+H2O +Mg(OH)Br(碱式溴化镁);
+Mg(OH)Br(碱式溴化镁);
| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 | -30.7°C | 156.2°C | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 | -34.6°C | 212.6°C | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,不溶于醇、醚等有机溶剂 | |
| 粗产品 | ① 操作 | ②溶解、过滤 | ③洗涤、干燥 | 三苯甲醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是物质的数量单位 | |
| B. | 58.5 gNaCl溶解在1 L水中,得到溶液的物质的量浓度为1mol/L | |
| C. | 标况下,1 mol CCl4 所占的体积约为22.4 L | |
| D. | 12g12C含有的碳原子数约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
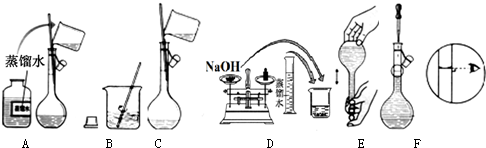
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 苯环中含有单双键交替的化学键 | |
| B. | 苯不能使酸性高锰酸钾溶液和溴水褪色 | |
| C. | 苯的化学性质没显示出极不饱和的性质,其性质与烯烃有很大的差别 | |
| D. | 苯在氢气气存在的情况下可以发生如下转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 可逆反应aA(g)+bB(s)?cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )
可逆反应aA(g)+bB(s)?cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )| A. | 温度降低,化学平衡向逆反应方向移动 | |
| B. | 使用催化剂,C的物质的量分数增加 | |
| C. | 化学方程式系数a<c+d | |
| D. | 无法根据图象确定改变温度后化学平衡移动方向 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com