
下列有关原电池的说法中,正确的是( )
| A.铝片和镁片用导线连接后插入NaOH溶液中,镁片较活泼,作负极 |
| B.铝片和铜片用导线连接后插入浓硝酸中,铜作负极 |
| C.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| D.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用锌片作负极,铁片作正极,FeCl3溶液作电解质 |
B
解析试题分析:A.铝片和镁片用导线连接后插入NaOH溶液中,由于Al能够与NaOH反应,而Mg不反应,所以Al片作负极。错误。B.铝片和铜片用导线连接后插入浓硝酸中,由于Al在常温下在浓硝酸中会发生钝化现象,所以铜作负极。正确。C.镀锌铁镀层破损后,由于活动性Zn>Fe,所以Zn作原电池的负极,首先被腐蚀,仍然对Fe起到保护作用;而镀锡铁的镀层破损后,由于活动性Fe>Sn,所以Fe最原电池的负极,首先被腐蚀,Fe腐蚀的比前者快。错误。D.若将反应2Fe3++Fe=3Fe2+设计为原电池,则可用铁片作负极,石墨作正极,FeCl3溶液作电解质。错误。
考点:考查原电池的电极材料的选择及金属的腐蚀的快慢半径的知识。


科目:高中化学 来源: 题型:单选题
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。则下列说法正确的是( )
| A.电池工作时,MnO2发生还原反应 |
| B.电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH- |
| C.电池工作时,K+移向负极 |
| D.电池工作时,电路中每通过0.1mol电子,锌的质量理论上减少6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于原电池的叙述正确的是( )
| A.构成原电池的正极和负极必须是两种不同金属 |
| B.原电池是把化学能转变为电能的装置 |
| C.在铅、银和盐酸构成的原电池工作时,铅板上有5.18 g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D.原电池工作时,正极和负极上发生的都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是 ( )
| A.H2SO4 | B.AgNO3 | C.Na2SO4 | D.NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
| A.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 |
| B.电池负极反应式为:O2 + 2H2O + 4e—= 4OH— |
| C.电解后c(Na2CO3)不变,且溶液中有晶体析出 |
| D.电池中c(KOH)不变;电解池中溶液pH变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是: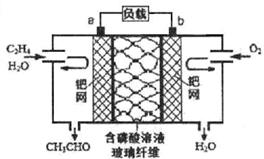
| A.该电池为可充电池 |
| B.每有0.1molO2反应,则迁移0.4mol |
| C.正极反应式为:CH2=CH2-2e-+2OH-=CH3CHO+H2O |
| D.电子移动方向:电极a→磷酸溶液 →电极b |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
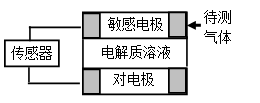
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是
| 待测气体 | 部分电极反应产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com