
分析 (1)根据n=$\frac{V}{{V}_{m}}$计算HxR气体的物质的量,再结合M=$\frac{m}{n}$计算相对分子质量;
(2)5.1gHxR气体的物质的量为0.15mol,CuSO4的物质的量也是0.15mol,二者等物质的量反应,则发生反应:HxR+CuCl2═CuR↓+2HCl,结合原子守恒计算x的值,进而确定R元素.
解答 解:(1)标况下,HxR气体的物质的量=$\frac{5.6L}{22.4L/mol}$=0.25mol,则其摩尔质量=$\frac{8.5g}{0.25mol}$=34g/mol,摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为34,
答:HxR的相对分子质量为34;
(2)n(HxR)=$\frac{5.1g}{34g/mol}$=0.15mol,而200mL 0.75mol•L-1的CuCl2溶液中氯化铜的物质的量为:0.2L×0.75mol•L-1=0.15mol,二者等物质的量反应,则发生反应:HxR+CuCl2═CuR↓+2HCl,由氢元素和氯元素质量守恒可知x=2,则Ar(R)=34-2=32,故R原子的质量数为32,且CuR为黑色沉淀,可推知R为硫元素,
答:x为2,R为硫元素.
点评 本题考查物质的量有关计算、化学方程式计算等知识点,难度不大,注意对基础知识的掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 它是苯酚的同系物 | |
| B. | 1mol该有机物能与溴水反应消耗2molBr2发生取代反应 | |
| C. | 1mol该有机物能与金属钠反应产生0.5molH2 | |
| D. | 1mol该有机物能与2molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
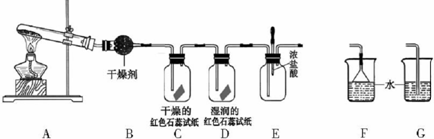
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对燃烧现象的深入研究 | B. | 对空气组成的研究 | ||
| C. | 用原子--分子论来研究化学反应后 | D. | 英国科学家汤姆生发现电子后 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质 Cl2、Br2、I2的氧化性强弱 | |
| B. | 气态氢化物 NH3、H2O、HF 的稳定性 | |
| C. | 碱金属单质 Li、Na、K 与水反应的剧烈程度 | |
| D. | 1mol Na、Mg、Al 分别与足量盐酸反应时失电子数的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
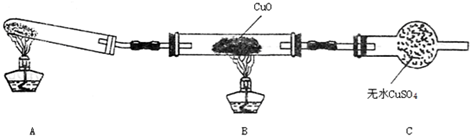
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com