
【题目】“8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究。
探究氰化物的性质:已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
25℃电离平衡常数 | Ki=1.77×10﹣4 | Ki=5.0×10﹣10 | Ki1=4.3×10﹣7 Ki2=5.6×10﹣11 |
(1)NaCN溶液呈碱性的原因是________________________ (用离子方程式表示)
(2)如图表示常温下,稀释HCOOH、HCN两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是_________

A.相同浓度的HCOONa和NaCN的混合溶液中,各离子浓度的大小关系是:c(Na+)>c(CN﹣)>c(HCOO﹣)>c(OH﹣)>c(H+)
B.向NaCN溶液中通入少量二氧化碳的离子方程式为:CN﹣+CO2+H2O=HCN+CO32﹣
C.图像中a点酸的总浓度小于b点酸的总浓度
D.c点溶液的导电性比a点溶液的导电性弱
(3)H2O2有“绿色氧化剂”的美称;也可消除水中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O═A+NH3↑,则生成物A的化学式为_____。
(4)下列四种离子结合H+能力由弱到强的是______________________________________。
A. HCOO- B. CN- C. CO32- D.HCO3-
【答案】CN﹣+H2OHCN+OH﹣ CD KHCO3 A<D<B<C
【解析】
(1)NaCN为强碱弱酸盐,CN-发生水解:CN-+H2O![]() HCN+OH-,c(OH-)>c(H+),使溶液显碱性;
HCN+OH-,c(OH-)>c(H+),使溶液显碱性;
(2)A、根据表中数据,酸性:HCOOH>HCN,即CN-水解程度大于HCOO-,离子浓度大小顺序是c(Na+)>c(HCOO-)>c(CN-)>c(OH-)>c(H+),故A错误;
B、电离出H+能力:H2CO3>HCN>HCO3-,通入少量CO2反应离子方程式为:CN-+CO2+H2O=HCN+HCO3-,故B错误;
C、根据表格数据,HCOOH的酸性强于HCN,相同pH时,稀释相同倍数,酸性强的pH变化大,即曲线I代表HCOOH,开始时pH相同,c(HCOOH)>c(HCN),故C正确;
D、电解质溶液导电能力与离子浓度、所带电荷数有关,c点离子浓度小于a点,即c点溶液的导电性比a点溶液的导电性弱,故D正确;
(3)利用原子守恒,推出A的化学式为KHCO3;
(4)根据表格中数据,电离出H+能力:HCOOH>H2CO3>HCN>HCO3-,利用越弱越水解,推出结合H+能力由弱到强的顺序是HCOO-<HCO3-<CN-<CO32-,即A<D<B<C。


科目:高中化学 来源: 题型:
【题目】硼、铝、镓、铟、铊是第ⅢA族元素,它们在工农业生产中应用非常广泛。
(1)基态硼原子的核外电子排布图为______________________。
(2)I1(Mg)___________I1(Al)(填“大于”或“小于”),其原因是______________________。
(3)三氯化铝加热到177.8℃时,会升华为气态二聚氯化铝(Al2Cl6,其中铝原子和氯原子均达8电子稳定结构),请写出二聚氯化铝(Al2Ci6)的结构式:______________________,其中铝原子轨道采用___________杂化。
(4)BF4-的空间构型为___________,与BF4-互为等电子体的分子是___________ (写化学式,任写一种即可)。
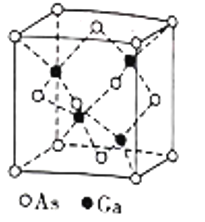
(5)镓(Ga)可与砷(As)形成砷化(GaAs)晶体,该晶体的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________。Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,阿伏加德罗常数值为NA,则晶胞中Ca与As原子的核间距为___________pm。(列出字母表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)是应用广泛、性能较好的还原剂,以硼酸、甲醇和氢化钠(NaH)为原料可制得硼氢化钠。某学习小组的同学欲利用下图所示路线在实验室合成硼氢化钠。

I.氢化钠的制备
已知NaH的化学反应活性很高,在潮湿的空气中能自燃,与酸接触即放出热量和氢引发燃烧甚至爆炸。该小组的同学利用下图中的装置在实验室制取NaH。

(1)NaH中氢元素的化合价为___________,NaH的电子式为___________。
(2)按气流方向连接各仪器接口,顺序为a→___________b→c(填接口字母);连接装置后进行实验,在给装置B加热前,必须进行的一步操作是___________。
(3)装置A中盛装稀盐酸的仪器名称为___________,装置D中应盛装的试剂是___________。
(4)经分析,该实验装置有一个明显的不足是____________,解决此不足的措施是__________。
Ⅱ.硼氢化钠的制备与纯度测定
在搅拌加热到220℃时,向盛装NaH的缩合反应罐中加入硼酸三甲酯[B(OCH3)3],升温到260℃,充分反应后,经过处理得到NaBH4和甲醇钠。
(5)某同学欲通过测定硼氢化钠与水反应生成氢气的体积来测定硼氢化钠产品的纯度。
已知:NaH+H2O=H2↑+NaOH。
①硼氢化钠与水反应可以产生大量氢气和偏硼酸钠,该反应方程式为___________。
②该同学用图装置测定硼氢化钠产品的纯度(杂质只有氢化钠)。装置中a的作用是_________;称取6.28g氢化钠样品,重复实验操作三次,测得生成气体的平均体积为13.44L(已折算为标准状况),则样品中硼氢化钠的纯度为___________%(结果保留两位有效数字)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
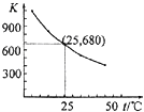
A. 反应I2(aq)+I-(aq)![]() I3 -(aq)的ΔH>0
I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,改变0.1mol·L-1H2SO3溶液的pH,各微粒的物质的量分数(α)变化如图所示,下列说法中错误的是
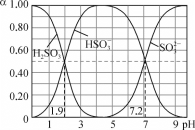
A. 1gK1(H2SO3)=-1.9
B. pH=3时,c(HSO3-)>c(H2SO3)>c(SO32-)
C. 反应H2SO3+SO32-![]() 2HSO3-的lgK=5.3
2HSO3-的lgK=5.3
D. pH=7.2时,c(HSO3-)=c(SO32-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中常含有少量的泥沙及氯化钙、氯化镁、硫酸盐等一些可溶性的杂质。粗盐的提纯实验操作步骤如图所示:
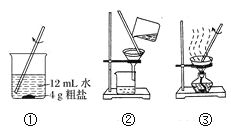
(1)请写出图中各步实验操作的名称②_____,③______。
(2)实验操作②的主要目的是______。
(3)实验操作①②③中都使用的仪器是_____,它在③中其作用是_____。
(4)通过上述实验操作,得到的精盐中可能含有的杂质是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A. 该溶液的pH=4 B. 升高温度,溶液的pH增大 C. 此酸的电离平衡常数约为1×10-7 D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,浓度均为0.1mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 |
|
|
|
|
pH | 7.0 | 7.0 | 8.1 | 8.9 |
A. 酸性强弱: ![]()
B. 离子的总浓度:①>③
C. ②中: ![]()
D. ②和④中![]() 相等
相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com