
下列化学用语的相关表述正确的是
A.H+(aq)+OH-(aq)=H2O(l) △H=-a kJ/mol,故1 mol NaOH固体与足量的稀盐酸反应,放出热量为a kJ
B.因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H=+b kJ/mol,故1 mol CuSO4(s)溶于足量水时,放出热量为b kJ
C.因氢气的燃烧热为c kJ/mol,故电解水的热化学方程式为:2H2O(1)=2H2(g)+O2(g)△H=+c kJ/mol
D.因N2(g)+3H2(g) 2NH3(g) △H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ
2NH3(g) △H=-d kJ/mol,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ
【答案】D
【解析】
试题分析:H+(aq)+OH-(aq)=H2O(l) △H=-a kJ/mol,说明1 mol NaOH稀溶液与足量的稀盐酸反应,放出热量为a kJ,A错误;CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H=+b kJ/mol,说明蓝帆受热分解时,放出热量为b kJ,B错误;因氢气的燃烧热为c kJ/mol,故电解水的热化学方程式为:2H2O(1)=2H2(g)+O2(g)△H=+2c kJ/mol,C错误;N2(g)+3H2(g) 2NH3(g) △H=-d kJ/mol,因该反应为可逆反应,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ,D正确。
2NH3(g) △H=-d kJ/mol,因该反应为可逆反应,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出热量小于d kJ,D正确。
考点:考查化学用语等知识。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
A.1∶4 B.1∶5
C.2∶3 D.2∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阿伏加德罗常数的说法正确的是( )
A.阿伏加德罗常数是国际单位制中七个基本物理量之一
B.1 mol任何物质都约含有6.02×1023个原子
C.阿伏加德罗常数约为6.02×1023 mol-1
D.阿伏加德罗常数没有单位
查看答案和解析>>
科目:高中化学 来源: 题型:
实验是化学研究的基础。下列关于各实验装置的叙述正确的是( )
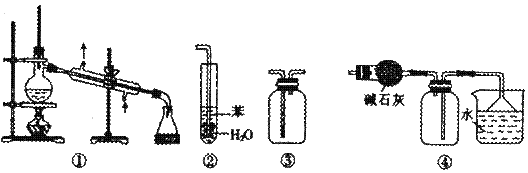
A.装置①常用于分离互不相溶的液体混合物
B.装置②可用于吸收NH3或HCl气体,并防止倒吸
C.装置③可用于收集H2、CO2、Cl2、NH3等气体
D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关物质的电离平衡常数:
| 弱酸 | CH3COOH | 苯酚 | H2CO3 |
| 电离平衡常数 | 1.75×l0–5 | 1.1×l0–10 | K1=4.4×l0–7 K2=4.7×l0–11 |
下列叙述错误的是
A.等物质的量浓度的各溶液pH关系为:
pH(C6H5ONa)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa)
B.向苯酚钠溶液中通入少量CO2气体反应为:C6H5O– +H2O + CO2 →C6H5OH +HCO3-
C.等物质的量浓度的苯酚稀溶液与 NaOH稀溶液等体积混合后溶液中:
c(Na+)>c(C6H5O–)>c(OH–)>c(H+)
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–)
查看答案和解析>>
科目:高中化学 来源: 题型:
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
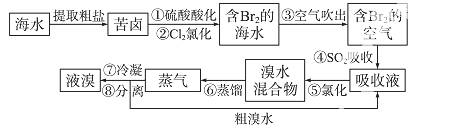
(1)溴在周期表中位于第 _周期第 _族。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,理由是 _。
(3)步骤④利用了SO2的还原性,反应的离子方程式为 _。
(4)步骤⑥的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因 _。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是 _。
(6)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是 _。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H+(aq)+OH-(aq)====H2O(l) ΔH=-57.3 kJ·mol-1。对于下列反应:
①HCl(aq)+NH3·H2O(aq)====NH4Cl(aq)+H2O(l) ΔH=-a kJ·mol-1
②HNO3(aq)+KOH(aq)====KNO3(aq)+H2O(l) ΔH=-b kJ·mol-1
则a、b的大小关系为( )
A.a>b B.b>a
C.a=b D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
将等体积的AlCl3和NaOH溶液混合,充分反应后,发现铝元素有一半形成了沉淀,则此时铝元素的存在形式为( )
①Al3+和Al(OH)3 ②[Al(OH)4]-和Al(OH)3 ③Al3+和Al2O3 ④[Al(OH)4]-和Al2O3
A.①② B.②③ C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com