
”¾ĢāÄæ”æøł¾ŻĪŹĢā½ųŠŠ¼ĘĖć£ŗ
£Ø1£©ŹµŃé²āµĆ16g¼×“¼[CH3OH£Øl£©]ŌŚŃõĘųÖŠ³ä·ÖČ¼ÉÕÉś³É¶žŃõ»ÆĢ¼ĘųĢåŗĶŅŗĢ¬Ė®Ź±ŹĶ·Å³ö363.25kJµÄČČĮ棬ŹŌŠ“³ö¼×“¼Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½£ŗ £®
£Ø2£©“Ó»Æѧ¼üµÄ½Ē¶Č·ÖĪö£¬»Æѧ·“Ó¦µÄ¹ż³Ģ¾ĶŹĒ·“Ó¦ĪļµÄ»Æѧ¼ü±»ĘĘ»µŗĶÉś³ÉĪļµÄ»Æѧ¼üµÄŠĪ³É¹ż³Ģ£®ŅŃÖŖ·“Ó¦£ŗN2£Øg£©+3H2£Øg£©2NH3£Øg£©”÷H=a kJmol©1 £® ÓŠ¹Ų¼üÄÜŹż¾ŻČē±ķ£ŗ
»Æѧ¼ü | H©H | N©H | N”ŌN |
¼üÄÜ£ØkJmol©1£© | 436 | 391 | 945 |
ŹŌøł¾Ż±ķÖŠĖłĮŠ¼üÄÜŹż¾Ż¹ĄĖćaµÄŹżÖµ £®
£Ø3£©ŅĄ¾ŻøĒĖ¹¶ØĀÉæÉŅŌ¶ŌijŠ©ÄŃŅŌĶعżŹµŃéÖ±½Ó²ā¶ØµÄ»Æѧ·“Ó¦µÄ·“Ó¦ČČ½ųŠŠĶĘĖć£®ŅŃÖŖ£ŗ
C£Øs£¬ŹÆÄ«£©+O2£Øg£©ØTCO2£Øg£©”÷H1=©393.5kJmol©1
2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H2=©571.6kJmol©1
2C2H2£Øg£©+5O2£Øg£©ØT4CO2£Øg£©+2H2O£Øl£©”÷H3=©2599kJmol©1
øł¾ŻøĒĖ¹¶ØĀÉ£¬¼ĘĖć298KŹ±ÓÉC£Øs£¬ŹÆÄ«£©ŗĶH2£Øg£©Éś³É1mol C2H2£Øg£©·“Ó¦µÄ·“Ó¦ČČĪŖ£ŗ”÷H= £®
£Ø4£©ŌŚĪ¢ÉśĪļ×÷ÓƵÄĢõ¼žĻĀ£¬NH4+¾¹żĮ½²½·“Ó¦±»Ńõ»Æ³ÉNO3© £® Į½²½·“Ó¦µÄÄÜĮæ±ä»ÆŹ¾
ŅāĶ¼ČēĶ¼£ŗ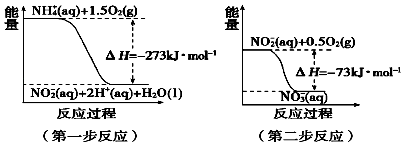
µŚŅ»²½·“Ó¦ŹĒ·“Ó¦£ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©£¬ŌŅņŹĒ £®
”¾“š°ø”æ
£Ø1£©CH3OH £Øl£©+ ![]() O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=©726.5KJ/mol
O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=©726.5KJ/mol
£Ø2£©©93
£Ø3£©+226.7 KJ/mol
£Ø4£©·ÅČČ,·“Ó¦Īļ×ÜÄÜĮæøßÓŚÉś³ÉĪļ×ÜÄÜĮæ
”¾½āĪö”æ½ā£ŗ£Ø1£©16gCH3OHŌŚŃõĘųÖŠČ¼ÉÕÉś³ÉCO2ŗĶŅŗĢ¬Ė®£¬·Å³ö363.25kJČČĮ棬32g¼“1molCH3OHŌŚŃõĘųÖŠČ¼ÉÕÉś³ÉCO2ŗĶŅŗĢ¬Ė®£¬·Å³ö726.5kJČČĮ棬Ōņ”÷H=©726.5KJ/mol£¬ŌņČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCH3OH £Øl£©+ ![]() O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=©726.5KJ/mol£¬
O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=©726.5KJ/mol£¬
ĖłŅŌ“š°øŹĒ£ŗCH3OH £Øl£©+ ![]() O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=©726.5KJ/mol£»
O2£Øg£©=CO2£Øg£©+2H2O£Øl£©”÷H=©726.5KJ/mol£»
£Ø2£©N2£Øg£©+3H2£Øg£©2NH3£Øg£©”÷H=945kJmol©1+436kJmol©1”Į3©391kJmol©1”Į6=©93kJmol©1=a kJmol©1£¬Ņņ“Ėa=©93£¬
ĖłŅŌ“š°øŹĒ£ŗ©93£»
£Ø3£©ŅŃÖŖ£ŗ¢ŁC £Øs£¬ŹÆÄ«£©+O2£Øg£©=CO2£Øg£©”÷H1=©393.5kJmol©1£»
¢Ś2H2£Øg£©+O2£Øg£©=2H2O £Øl£©”÷H2=©571.6kJmol©1£»
¢Ū2C2H2£Øg£©+5O2£Øg£©ØT4CO2£Øg£©+2H2O £Øl£©”÷H2=©2599kJmol©1£»
2C £Øs£¬ŹÆÄ«£©+H2£Øg£©=C2H2£Øg£©µÄ·“Ó¦æÉŅŌøł¾Ż¢Ł”Į2+¢Ś”Į ![]() ©¢Ū”Į
©¢Ū”Į ![]() µĆµ½£¬
µĆµ½£¬
ĖłŅŌ·“Ó¦ģŹ±ä”÷H=2”Į£Ø©393.5kJmol©1£©+£Ø©571.6kJmol©1£©”Į ![]() ©£Ø©2599kJmol©1£©”Į
©£Ø©2599kJmol©1£©”Į ![]() =+226.7kJmol©1£¬
=+226.7kJmol©1£¬
ĖłŅŌ“š°øŹĒ£ŗ+226.7 KJ/mol£»
£Ø4£©ŅņĪŖ”÷H=©273kJ/mol£¼0£¬Ōņ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬
ĖłŅŌ“š°øŹĒ£ŗ·ÅČČ£¬·“Ó¦Īļ×ÜÄÜĮæøßÓŚÉś³ÉĪļ×ÜÄÜĮ森
”¾æ¼µć¾«Īö”æ¹ŲÓŚ±¾Ģāæ¼²éµÄ·“Ó¦ČČŗĶģŹ±ä£¬ŠčŅŖĮĖ½āŌŚ»Æѧ·“Ó¦ÖŠ·Å³ö»ņĪüŹÕµÄČČĮ棬Ķس£½Š·“Ó¦ČČ²ÅÄÜµĆ³öÕżČ·“š°ø£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓ¦¶ŌÄÜŌ“Ī£»śµÄÓŠŠ§Ķ¾¾¶Ö®Ņ»¾ĶŹĒŃ°ÕŅŠĀÄÜŌ“£®ĻĀĮŠŹōÓŚŠĀÄÜŌ“µÄŹĒ£Ø £©
A.Ćŗ
B.ŹÆÓĶ
C.Ģ«ŃōÄÜ
D.ĢģČ»Ęų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧÓėÉś»ī”¢Éś²śĆÜĒŠĻą¹Ų”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. õ„ŌŚ¼īŠŌĢõ¼žĻĀµÄĖ®½ā·“Ó¦½ŠŌķ»Æ·“Ó¦![]()
B. Ļš½ŗ”¢ŗĻ³ÉĖÜĮĻ”¢ŗĻ³ÉĻĖĪ¬¾łŹĒČĖ¹¤ŗĻ³ÉµÄøß·Ö×Ó²ÄĮĻ
C. ¹Å“śĖÄ“ó·¢Ć÷ÖŠ”°ŗŚ»šŅ©”±µÄ³É·ÖŹĒ”°Ņ»Įņ¶žĻõČżÄ¾Ģæ”±£¬ÕāĄļµÄ”°Ļõ”±ÖøµÄ×ćĻõĖį
D. ”¶Ģģ¹¤æŖĪļ”·¼ĒŌŲ£ŗ”°·²ŪļÄąŌģĶߣ¬¾ņµŲ¶ž³ßÓą£¬ŌńČ”ĪŽÉ³Õ³ĶĮ¶ųĪŖÖ®”±”£”°Ķß”±£¬“«Ķ³ĪŽ»ś·Ē½šŹō²ÄĮĻ£¬Ö÷ŅŖ³É·ÖĪŖ¹čĖįŃĪ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æȔȿÕÅĄ¶É«ŹÆČļŹŌÖ½·ÅŌŚ²£Į§Ę¬ÉĻ£¬Č»ŗó°“Ė³Šņ·Ö±šµĪ¼Ó65%µÄHNO3”¢98%µÄH2SO4ŗĶŠĀÖʵÄĀČĖ®£¬ČżÕÅŹŌÖ½³ŹĻÖµÄŃÕÉ«·Ö±šŹĒ£Ø £©
A.°×”¢ŗģ”¢°×
B.ŗģ”¢ŗŚ”¢°×
C.ŗģ”¢ŗģ”¢ŗģ
D.°×”¢ŗŚ”¢°×
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪļÖŹAŹĒÉś²śø÷ÖÖĖÜĮĻµÄÖŲŅŖµ„Ģ壬¹¤ŅµÉĻ²ÉÓĆĪļÖŹB·Ö½āÖʱøĪļÖŹAµÄĶ¬Ź±ŹĶ·Å³öĒāĘų£¬ĘäÖʱøŌĄķŹĒ£ŗ
B£Øg£©A£Øg£©+H2£Øg£©”÷H=+125kJmol©1
£Ø1£©øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK= £® Ėę×ÅĪĀ¶ČµÄÉżøߣ¬KÖµ£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£®
£Ø2£©Źµ¼ŹÉś²śÖŠ³£ŅŌøßĪĀĖ®ÕōĘų×÷ĪŖ·“Ó¦ĢåĻµµÄĻ”ŹĶ¼Į£ØĻ”ŹĶ¼Į²»²Ī¼Ó·“Ó¦£©£®ĪļÖŹBµÄĘ½ŗā×Ŗ»ÆĀŹÓėĖ®ÕōĘųµÄÓĆĮ攢ĢåĻµ×ÜŃ¹Ēæ¹ŲĻµČēĶ¼£®
¢ŁÓÉĶ¼æÉµĆ³ö£ŗ
½įĀŪŅ»£ŗĘäĖūĢõ¼ž²»±ä£¬Ė®ÕōĘųµÄÓĆĮæŌ½“ó£¬Ę½ŗā×Ŗ»ÆĀŹŌ½£»
½įĀŪ¶ž£ŗ
¢Ś¼ÓČĖĻ”ŹĶ¼ĮÄÜÓ°Ļģ·“Ó¦ĪļBµÄĘ½ŗā×Ŗ»ÆĀŹµÄŌŅņŹĒ£ŗ £®
£Ø3£©Ä³Š©¹¤ŅÕÖŠ£¬ŌŚ·“Ó¦µÄÖŠĶ¾¼ÓČėO2ŗĶĢŲ¶ØµÄ“߻ƼĮ£¬ÓŠĄūÓŚĢįøßBµÄĘ½ŗā×Ŗ»ÆĀŹ£®ŹŌ½āŹĶĘäŌŅņ£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖÖŹĮæŹżĪŖAµÄijŃōĄė×ÓRn+ £¬ ŗĖĶāÓŠXøöµē×Ó£¬ŌņŗĖÄŚÖŠ×ÓŹżĪŖ£Ø £©
A.A©x
B.A©x©n
C.A©x+n
D.A+x©n
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£ŗ¼×·Ö×ÓŗĶŅŅ·Ö×Ó·“Ӧɜ³É±ū·Ö×ÓŗĶ¶”·Ö×Ó£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£© 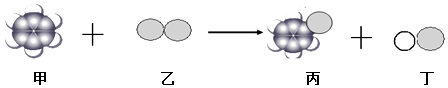
A.·ÖĄė¼×ŗĶ±ūæÉŅŌ²ÉÓĆÕōĮó·Ø
B.¼×µÄæռ乹ŠĶŹĒĘ½ĆęÕżĮł±ßŠĪ
C.±ū²»ŹōÓŚĢžĄąĪļÖŹ
D.øĆ·“Ó¦ĄąŠĶŹĒÖĆ»»·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĻĀĶ¼ĖłŹ¾×°ÖĆĶ¼£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
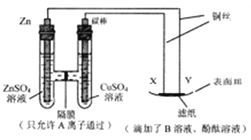
A. XÓėĀĖÖ½½Ó“„“¦µÄĶĖæ·¢Éś·“Ó¦Cu-2e-=Cu2+
B. Ģ¼°ō±ķĆęÖš½„Éś³ÉŗģÉ«ĪļÖŹ
C. ČōøōĤ×ó²ąČÜŅŗÖŠŹ¼ÖÕÖ»ÓŠŅ»ÖÖČÜÖŹ£¬ŌņAĄė×Ó²»ÄÜŹĒCu2+
D. ČōĀĖÖ½ÓėY½Ó“„“¦±äŗģ£¬ŌņBČÜŅŗæÉŅŌŹĒAgNO3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē½āÖŹČÜŅŗµ¼µēÄÜĮ¦Ō½Ē棬µēµ¼ĀŹŌ½“󔣳£ĪĀĻĀÓĆ0.1000 mol/L ŃĪĖį·Ö±šµĪ¶Ø10.00 mLÅØ¶Č¾łĪŖ0.1000 mol/LµÄNaOHČÜŅŗŗĶ¶ž¼×°·[ (CH3)2NH]ČÜŅŗ( ¶ž¼×°·ŌŚĖ®ÖŠµēĄėÓė°±ĻąĖĘ£¬ŅŃÖŖŌŚ³£ĪĀĻĀKb[(CH3)2NH”¤H2O] =1.6”Į10-4)£¬ĄūÓĆ“«øŠĘ÷²āµĆµĪ¶Ø¹ż³ĢÖŠČÜŅŗµÄµēµ¼ĀŹČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
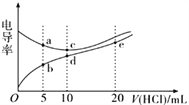
A. ŃĪĖįµĪ¶Ø¶ž¼×°·ŹµŃéÖŠŃ”Ōń·ÓĢŖ×öÖøŹ¾¼Į±ČŃ”¼×»ł³ČĪó²īøüŠ”
B. dµćČÜŅŗÖŠ£ŗc(H+)<c(OH-)+c[(CH3)2NH2+]
C. a µćČÜŅŗÓėdµćµÄČÜŅŗ»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc[(CH3)2NH2+]<c[(CH3)2NH”¤H2O]
D. b”¢c”¢e.ČżµćµÄČÜŅŗÖŠ£¬Ė®µÄµēĄė³Ģ¶Č×ī“óµÄŹĒeµć
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com