
A��B��C��D��EΪ��ѧ��ѧ�����ĵ��ʻ�����ת����ϵ����ͼ��ʾ��
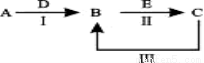
��1����A�ǵ���ɫ�����������D����ɫ���壻C�к��е����������Ӿ�Ϊ10�������ӡ�
��д����ӦA��B�Ļ�ѧ����ʽ ��
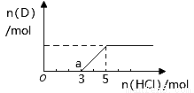
����һ����������Dͨ��2 L C����Һ�У���������Һ�б���μ���ϡ����������������������������������ʵ����Ĺ�ϵ��ͼ������������ܽ��HCl�Ļӷ�������ش�O����Һ���������ʵĻ�ѧʽΪ ��a����Һ�и�����Ũ���ɴ�С�Ĺ�ϵ�� ��
��2��������1���е�����Dͨ������������Һ�еò�����F��F��KSP=8.1��10-9���ֽ��ó�������0.1mol/L ��BaCl2��Һ�У���KSP ���������С�� �䣩����ɲ�����F������������Һ�е�Ũ��Ϊ mol/L��
��1��2CO2 + 2Na2O2�� 2Na2CO3 + O2 (3��)NaOH��Na2CO3 (2��)
c(Na+)��c(Cl-)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-) (3��)
��2������ (2��) �� 8.1��10-8 (2��)
��������
����������������Ϲ�ϵͼȷ��AΪ����������BΪ̼������CΪ��������������A��B��ѧ����ʽΪ2CO2 + 2Na2O2�� 2Na2CO3 + O2 ����̼���������ᷴӦ���ص�Na2CO3+HCl=NaHCO3+NaCl��NaHCO3+HCl=NaCl+H2O+CO2������������ͬ��������������ȷ��ͼ��O�������ΪNaOH��Na2CO3 ��a ��Ϊ3molNaCl��2molNaHCO3,����Ũ�ȴ�СΪ c(Na+)��c(Cl-)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-) ��Kspֻ���¶�Ӱ�������Բ�������c��SO42-��=Ksp��BaSO4��/c(Ba2+)=8.1��10-8.
���㣺�ƵĻ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и߶���ѧ��ѧҵˮƽģ�⻯ѧ�Ծ��������������棩 ���ͣ������
��ѧ����ᾭ�ý��衢��̬�������衢���ཡ�����ϵ�������ء�
��1�������Ǿ��ú���̬�����������Ҫ���ʻ�����
������������ˮ�����ͨ���������õ��Ĺ�ͬԭ���� ��
������������̥����Ҫԭ�ϣ������� ������ĸ����
A���������� B�����ǽ������� C���л��߷��Ӳ���
��������Ʒ�ڳ�ʪ�Ŀ������ܷ��� ��ʴ�������ø�ʴʱ�ĸ�����ӦʽΪ ��
��2�����λ�����Ⱦ��������̬�����ѳ�Ϊȫ��ʶ��
��2013�꣬ȫ�����ʡ�г������ص��������������������γɵ���Ҫ��Ⱦ���� (����ĸ)��
A��O2 B��CO2 C��PM2.5
�����÷��մ����������з������ڽ���Ͷ��ʹ�á������������еij�������.
A���ϵ�� B�������� C������ƿ
�ڷ��մ���ǰ�����ϵ���⣬���� ������ĸ��Ӧ�������գ����ⶪ�������ɵ���ҪΣ���� ��
��Ư�ۿ�����������ˮ��ɱ����������ҵ������������ʯ������ȡƯ�۵Ļ�ѧ��Ӧ����ʽ�� ��
��3����5�֣���֤ʳƷ��ȫ������Ӫ�����⣬�DZ������彡���Ļ�����
��ά����C�ܴٽ������������������и���ά����C���� ������ĸ����
A��ţ�� B������ C������
��ȱ��ij����Ԫ�ؽ����¼�״���״����������������Ԫ����
A���� B���� C����
�������ڵ������ڵ���ø�����£�ˮ��Ϊ ���ڼ�������Һ�м��뱥���������Һ�г��������Ĺ��̳�Ϊ ��
��ʹ����ù�ؿ��ܻ��������������ҩǰ����һ��Ҫ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ���ѡ�ޣ��������棩 ���ͣ�ѡ����
�����л���������ȷ����
A��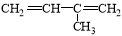 3������1��3������ϩ
3������1��3������ϩ
B��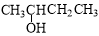 2���ǻ�����
2���ǻ�����
C��CH3CH(C2H5)CH2CH2CH3 2���һ�����
D��CH3CH(CH3)CH2COOH 3��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ������ޣ��������棩 ���ͣ�ѡ����
����ʵ��װ�á��Լ�ѡ�û������ȷ����
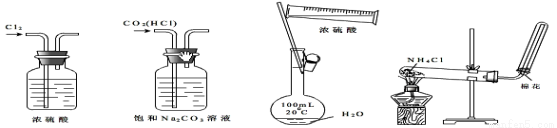
A������Cl2 B����ȥCO2�е�HCl C��ϡ��Ũ���� D����ȡ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ������ޣ��������棩 ���ͣ�ѡ����
�������������ڷǵ���ʵ���
A��BaSO4 B��NaOH C��Na2O2 D��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ��ͬ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼ��ʾʵ��װ�õ�K�պϣ������ж���ȷ����
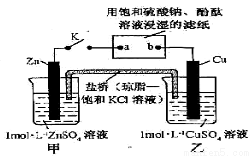
A�� �缫�Ϸ�����ԭ��Ӧ
�缫�Ϸ�����ԭ��Ӧ
B��������Zn a
a b
b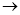 Cu·������
Cu·������
C��Ƭ�̺�׳���c��SO42��������
D��Ƭ�̺�ɹ۲쵽��ֽb����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ��ͬ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��̬��1 mol����2 mol HCl��ȫ�ӳɣ��ӳɺ��������ϵ���ԭ���ֿɱ�6 mol Cl2ȡ���������̬��������
A��CH3��C��C��CH3 B�� CH2��CH2
C��CH��C��CH3 D��CH2��CH��CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и߶�3���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ȷ���� ( )
A��CS2ΪV�η���
B��NCl3�Ŀռ乹��Ϊƽ��������
C�����ĵ�һ�����ܱ�þ�ĵ�һ�����ܴ�
D��SiF4��H2O������ԭ�Ӿ�Ϊsp3�ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015������к������߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ͼ��п�̵�أ�����˵����ȷ����
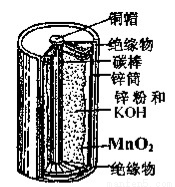
A��MnO2����������������
B��̼��Ϊ������пͲΪ����
C���ŵ������NH4+��п���ƶ�
D��������ӦΪ��Zn-2e-+2OH-=Zn(OH)2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com