
【题目】根据下列框图回答问题(答题时方程式中的M、E用所对应的元素符号表示): 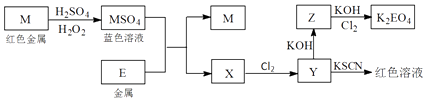
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: .
(2)写出X生成Y的离子方程式: .
(3)某同学取Y的溶液,酸化后加入KI淀粉溶液,溶液变为蓝色.写出与上述变化过程相关的离子方程式: .
(4)写出将Cl2通入足量氢氧化钾溶液中反应的离子方程式: .
【答案】
(1)Cu+H2O2+H2SO4═CuSO4+2H2O
(2)2Fe2++Cl2=2Fe3++2Cl﹣
(3)2Fe3++2I﹣=2Fe2++I2
(4)Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
【解析】解:(1)M为Cu,溶于稀H2SO4和H2O2混合液的化学方程式为Cu+H2O2+H2SO4═CuSO4+2H2O,
所以答案是:Cu+H2O2+H2SO4═CuSO4+2H2O;(2)X为FeSO4,X生成Y的离子方程式为2Fe2++Cl2=2Fe3++2Cl﹣,所以答案是:2Fe2++Cl2=2Fe3++2Cl﹣;(3)Y的溶液含Fe3+,酸化后加入KI淀粉溶液,溶液变为蓝色,可知离子反应为2Fe3++2I﹣=2Fe2++I2,所以答案是:2Fe3++2I﹣=2Fe2++I2;(4)Cl2通入足量氢氧化钾溶液中反应的离子方程式为Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,所以答案是:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O.


科目:高中化学 来源: 题型:
【题目】用铁和稀硫酸制氢气,不能加快氢气生成速率的措施是
A. 用等质量的铁粉代替铁片B. 用98%浓硫酸代替稀硫酸
C. 在稀硫酸中滴加少量CuSO4溶液D. 溶液加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关杂化轨道的叙述错误的是 ( )
A.并不是所有的原子轨道都参与杂化
B.同一个原子中能量相近的原子轨道参与杂化
C.杂化轨道能量集中,有利于牢固成键
D.杂化轨道中一定有电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于使用托盘天平的叙述,不正确的是
A. 称该前先调节托盘天平的零点
B. 称量时左盘放被称量物,右盘放砝码
C. 潮湿的或具有腐蚀性的药品,必须放在玻瑞器皿里称量,其他固体药品可直接放在天平托盘上称量
D. 用托盘天平可以准确称量至0.1g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙酸异戊酯的密度为0.8670g·cm-1,是难溶水的液体。在洗涤、分液操作中,应充分振荡,然后静置,待分层以后获得乙酸异戊酯的操作是
A. 直接将乙酸异戊酯从分液漏斗的上口倒出
B. 直接将乙酸异戊酯从分液漏斗的下口放出
C. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是( )
A.K2SO4
B.CH3COONa
C.CuSO4
D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
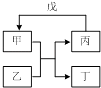
【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,满足如图所示转化关系的是( )
甲 | 乙 | 丙 | 戊 | |
A | Na2O2 | CO2 | O2 | Na |
B | Fe | H2O | Fe2O3 | H2 |
C | MgO | 盐酸 | MgCl2 | NaOH |
D | CuSO4 | Zn | Cu | 稀H2SO4 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A.H2O(g)=H2(g)+ ![]() O2(g)△H=+242kJmol﹣1
O2(g)△H=+242kJmol﹣1
B.2H2(g)+O2(g)=2H2O(l)△H=﹣484kJmol﹣1
C.H2(g)+ ![]() O2(g)=H2O(g)△H=+242kJmol﹣1
O2(g)=H2O(g)△H=+242kJmol﹣1
D.2H2(g)+O2(g)=2H2O(g)△H=+484kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子总数、价电子总数都相等的微粒称为等电子体。下列各组微粒中不能互称为等电子体的是 ( )
A.CH4、NH4+B.H2S、HCl
C.CO2、N2OD.CO、N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com