
科目:高中化学 来源:不详 题型:单选题
| A.NaOH | B.NaCl | C.HCl | D.Na2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
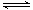 NO + SO3,在体积为VL的密闭容器中通入amolNO2和bmolSO2,反应后容器内硫原子和氧原子的个数比为( )
NO + SO3,在体积为VL的密闭容器中通入amolNO2和bmolSO2,反应后容器内硫原子和氧原子的个数比为( )A.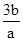 | B.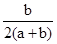 | C.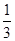 | D.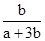 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
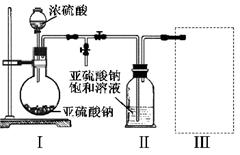
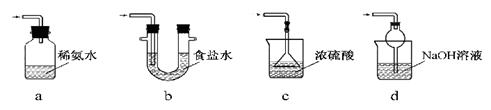

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
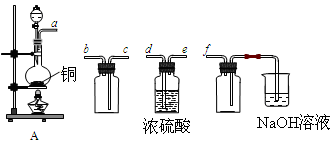
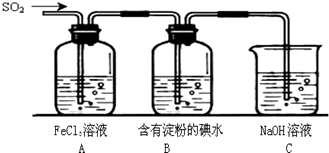
| A.烧瓶 | B.酒精灯 | C.漏斗 | D.烧杯 E.玻璃棒 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.点燃硫磺.产生刺激性气味气体,该气体可以漂白纸浆 |
| B.向蔗糖中加入浓硫酸,蔗糖变黑色,说明浓硫酸具有强的吸水性 |
| C.将H2S气体通入CuSO4溶液生成CuS沉淀,说明H2S为强电解质 |
| D.将Al片加入浓硫酸中,反应剧烈,说明浓硫酸具有强的氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜与浓硫酸反应所得白色固体不是CuSO4 |
| B.加BaCl2溶液后所得白色沉淀是BaSO3 |
| C.白色固体中夹杂的少量黑色物质可能是CuO |
| D.白色固体中夹杂的少量黑色物质中一定含有元素Cu和S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com