
| A. | NH4CO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | B. | 2Na2O2+2 H2O═4NaOH+O2↑ | ||
| C. | H2O+Cl2?HCl+HClO | D. | NH3+SO2+H2O═NH4HSO3 |
分析 活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,据此分析解答.
解答 解:A.该反应中有离子键和极性键的断裂和极性键的形成,没有离子键的形成和非极性键的断裂和形成,故A错误;
B.该反应中有非极性键的断裂、极性键的断裂、非极性键的断裂和离子键的形成、非极性键、极性键的形成,故B正确;
C.该反应中没有离子键的断裂和形成、没有非极性键的形成,故C错误;
D.该反应中没有离子键的断裂、非极性键的断裂和非极性键的形成,故D错误;
故选B.
点评 本题考查化学键,为高频考点,侧重考查基本概念,明确物质中存在的化学键是解本题关键,题目难度不大.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol Cl2所占体积约为11.2 L | |
| B. | 16 g O2中含有的分子数约为6.02×1023 | |
| C. | 0.1 mol/L NaCl溶液中含溶质的物质的量为0.1 mol | |
| D. | 标准状况下,11.2 L N2和CO的混合气体所含原子数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 草酸能使酸性高锰酸钾溶液褪色 | |
| B. | MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 | |
| C. | 要判断反应进行的方向,必须综合考虑体系的焓变和熵变 | |
| D. | 用稀硫酸和Zn反应制H2时,加少量CuSO4溶液对反应速率无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
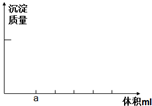 把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程.
把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程. 
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤、蒸馏、萃取 | B. | 过滤、结晶、升华 | C. | 分液、溶解、萃取 | D. | 溶解、过滤、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Fe与足量氧气反应时转移的电子数为2NA | |
| B. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为4NA | |
| D. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅含有碳、氢元素的有机物叫烃 | B. | 甲烷是最简单的有机物 | ||
| C. | 乙烷、丙烷均不存在同分异构体 | D. | 含碳元素的物质都是有机物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com