
 (2)第二周期第VIIA族
(2)第二周期第VIIA族 。
。

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.SO2的水溶液能够导电,但SO2是非电解质 |
| B.饱和氯水的导电性很好,所以氯气是强电解质 |
C. 和 和 为不同的核素,二者核外电子数不同 为不同的核素,二者核外电子数不同 |
| D.化合反应和分解反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可与活泼金属直接发生化学反应 | B.易溶于水也易溶于NaOH溶液 |
| C.是一种有毒气体 | D.可用HCN溶液与MnO2混合加热制取 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | X | | Y |
| Z | | W | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:W> Y> X |
| B.元素X与M形成化合物的空间构型可以是正四面体型、直线型或平面型等 |
| C.将X Z2通入W单质与水反应后的溶液中,生成的盐一定只有一种 |
| D.Y元素的含氧酸都属于强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

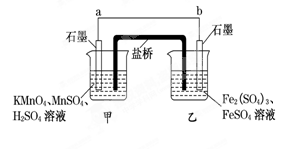
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com