
| A. | 2.4g镁变为镁离子失去的电子数为0.1NA | |
| B. | 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g | |
| C. | 标准状况下,2.24L四氯化碳含有分子的数目为0.1NA | |
| D. | 常温常压下,Na2O2与足量H2O反应,当生成0.2molO2时,转移电子的数目为0.4NA |
分析 A.一个镁原子失去2e-变为镁离子;
B.电解精炼铜时,阳极上是粗铜,粗铜上有其他金属杂质;
C.气体摩尔体积使用对象为气体;
D.Na2O2与H2O的反应是歧化反应;
解答 解:A.2.4g镁物质的量为0.1mol,变为镁离子失去的电子数为0.2NA,故A错误;
B.电解精炼铜时,阳极上是粗铜,粗铜上有其他比铜活泼的金属杂质也会放电,故阴极得到电子数为2NA时,阳极减少的质量不一定是64g,故B错误;
C.标况下,四氯化碳为液体,不能使用气体摩尔体积,故C错误;
D.Na2O2与H2O的反应是歧化反应:2Na2O2+2H2O=4NaOH+O2↑此反应转移2mol电子,生成1molO2,故当生成0.2molO2,转移电子0.4mol,数目为0.4NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,注意过氧化钠与水反应中,氧化剂、还原剂都是过氧化钠,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 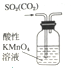 装置,除去SO2中混有的CO2 | |
| B. |  装置,用于亚硫酸钠和硫酸反应制取少量的SO2 | |
| C. | 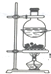 装置,分离NH4Cl和Ca(OH)2固体 | |
| D. | 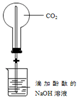 装置,做喷泉实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下列关于“瘦肉精”的说法中正确的是( )
下列关于“瘦肉精”的说法中正确的是( )| A. | 摩尔质量为305.5 | |
| B. | 属于芳香族化合物,也是高分子化合物 | |
| C. | 1mol该有机物在一定条件下可与3 mol氢气发生加成反应 | |
| D. | 向此有机物中加入硝酸酸化的硝酸银溶液会产生淡黄色的沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能量的释放或吸收是以发生变化的物质为基础的,二者密不可分,但以物质为主,如果物质没有变化,就不能引发能量的变化 | |
| B. | 氢能的优点是燃烧热值高,资源丰富,无毒无污染,且便于储存和运输,因此很可能成为未来的主要能源 | |
| C. | 对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 离子反应的速率决定于溶液中离子的浓度和离子的扩散速率,受温度影响不大,是一类不需要活化能来引发的反应,所以反应速率很高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
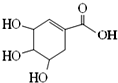
| A. | 分子式为C7H10O5 | |
| B. | 分子中含有3种官能团 | |
| C. | 可发生加成和取代反应 | |
| D. | 在水溶液中羟基和羧基均能电离出氢离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ①③⑤⑥⑦ | C. | ①②③④⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | N2$→_{放电}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
| B | NaCl(饱和)$→_{②CO_{2}}^{①NH_{3}}$NaHCO3$\stackrel{△}{→}$Na2CO3 |
| C | Fe$→_{点燃}^{少量Cl_{2}}$FeCl2$\stackrel{Cl_{2}}{→}$FeCl3 |
| D | FeS2$→_{煅烧}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com