
| A. | 该晶体类型是原子晶体 | |
| B. | 晶体中碳原子数与C-O化学键数之比为1:2 | |
| C. | 晶体的空间最小环共有6个原子构成 | |
| D. | 该晶体中碳原子和氧原子的个数比为1:2 |
分析 A.C原子和O原子结合为一种空间网状的无限伸展结构,所以构成该晶体的微粒是原子;
B.每个碳原子均以四个单键与氧原子结合;
C.每个碳原子均以四个共价单键与氧原子结合,该晶体的空间最小环由6个碳原子和6个氧原子构成;
D.该晶体中每个碳原子连接4个氧原子,则每个碳原子含有氧原子个数=$\frac{1}{2}$×4=2.
解答 解:A.C原子和O原子结合为一种空间网状的无限伸展结构,所以构成该晶体的微粒是原子,则为原子晶体,故A正确;
B.该晶体中,每个碳原子含有4个C-O共价键,所以C原子与C-O化学键数目之比为1:4,故B错误;
C.每个碳原子均以四个共价单键与氧原子结合,该晶体的空间最小环由6个碳原子和6个氧原子构成,所以每个最小环上含有12个原子,故C错误;
D.该晶体中每个碳原子连接4个氧原子,则每个碳原子含有氧原子个数=$\frac{1}{2}$×4=2,所以该晶体中碳原子和氧原子的个数比为1:2,故D正确;
故选BC.
点评 本题以碳氧化物为载体考查原子晶体,侧重考查学生空间想象能力及计算能力,利用均摊法计算即可,易错选项是C,题目难度中等.


科目:高中化学 来源: 题型:选择题
 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数.B原子核内质子数和中子数相等.下列叙述不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数.B原子核内质子数和中子数相等.下列叙述不正确的是( )| A. | C元素是非金属性最强的元素 | |
| B. | A元素最高价氧化物对应的水化物具有强氧化性 | |
| C. | 三种元素的原子半径的大小顺序是:B>C>A | |
| D. | B元素的氧化物、氢化物的水溶液都呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用布袋购物、以步代车属于“低碳生活”方式 | |
| B. | 饮用水中矿物质的含量越高越有利于人体健康 | |
| C. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 | |
| D. | 采用光触媒技术可将汽车尾气中的NO和CO转化为无毒气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号溶液 | 1 | 2 | 3 | 4 |
| KMnO4(mL) | 20.01 | 19.00 | 19.99 | 20.00 |
| Na2SO3(mL) | 25.00 | 25.00 | 25.00 | 25.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A. | 该反应的化学方程式是:H2(g)+CO2(g)?CO(g)+H2O(g) | |
| B. | 上述反应的正反应是吸热反应 | |
| C. | 如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,如果此时测得CO2为0.5 mol,则该反应达到平衡状态 | |
| D. | 某温度下,如果平衡常数符合下列关系式:$\frac{c(C{O}_{2})}{3c(CO)}$=$\frac{c({H}_{2}O)}{5c({H}_{2})}$,则此时温度700℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
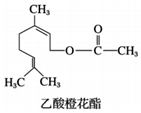 乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )| A. | ②④⑤ | B. | ①④⑤ | C. | ②③⑥ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向溶液中加入5 mL 0.01mol/L NaOH,所得溶液中离子的浓度一定符合:c(Na+)+c(H+)═c(OH-)+c(ClO-) | |
| B. | 25℃时,若溶液的pH=5,则Ka(HClO)=l×10-7 | |
| C. | 向溶液中加入少量NH4Cl固体,溶液中$\frac{c(HClO)}{c(Cl{O}^{-})}$的值变小 | |
| D. | 向溶液中加入10 mL O.01mol/L NaOH,所得溶液中离子浓度的大小顺序为:c(Na+)>c(ClO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
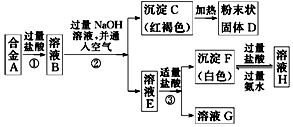 铁和铝是日常生活中用途广泛的金属.
铁和铝是日常生活中用途广泛的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{20}^{40}$Ca 和${\;}_{18}^{40}$Ar | B. | D和T | ||
| C. | H2 O和H2 O2 | D. | O3 和O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com