
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
分析 欲配制100mL 1.0mol/L Na2SO4溶液,需要硫酸钠的质量为:1.0mol/L×0.1L×142g/mol=14.2g;
需要Na2SO4•10H2O的质量为1.0mol/L×0.1L×322g/mol=32.2g,
溶于水配成100mL溶液,据此解答.
解答 解:①将14.2g Na2SO4溶于100mL水中,溶液的体积大于100mL,溶液的物质的量浓度小于1.0mol/L,故错误;
②32.2g Na2SO4•10H2O物质的量为0.1mol,溶于100mL水中,得到溶液的体积为100ml,溶液的物质的量浓度为0.1mol÷0.1L=1.0mol/L,故正确;
③设稀释后硫酸钠溶液浓度为c,根据稀释定律,稀释前后溶质硫酸钠的物质的量不变,则20ml×5mol/L=100ml×c,解得c=1mol/L,故正确;
故选:C.
点评 本题考查了配制一定物质的量浓度溶液,熟悉配制原理和过程是解题关键,注意溶液的体积与溶剂体积的差别,题目不难.


科目:高中化学 来源: 题型:解答题
| 实验 | 预期现象和结论 |
| 取少许吸收液于试管中滴加1~2滴0.01mol•L-1KMnO4溶液 | 若溶液褪色则假设1成立,否则假设1不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2倍 | B. | 1.5倍 | C. | 0.8倍 | D. | 0.5倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②③④ | C. | ①③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,它是由极性共价键形成的极性分子.
,它是由极性共价键形成的极性分子. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
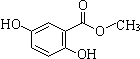
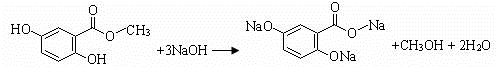 .(不用写反应条件)
.(不用写反应条件)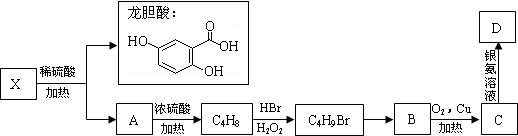
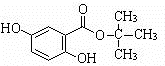 .
.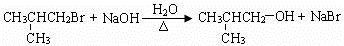 .(用结构简式表示)
.(用结构简式表示)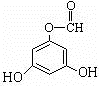 或
或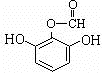 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用药匙取用粉末状或小颗粒状固体 | |
| B. | 用胶头滴管滴加少量液体 | |
| C. | 给盛有2/3体积液体的试管加热 | |
| D. | 过滤时漏斗的下端管口要紧靠烧杯内壁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com