
| A、由水电离产生的c(H+)=1×10-2mol?L-1溶液中,可能存在:CO32-、NH4+、Cl-,Na+ |
| B、某醋酸稀溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| C、Ba(OH)2溶液中加人过量的Al2(SO4)3溶液,其离子方程式为:3Ba2++60H-+2Al3++3SO42-=3BaS04↓+2Al(0H)3↓ |
| D、物质的量浓度均为1mol?L-1的NaCl和MgCl2混合液中,含有Cl-的数目为3NA(NA表示阿伏加德罗常数的值) |


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
 【化学--物质结构与性质】
【化学--物质结构与性质】 ;b.CH4; c.CH2=CHCH3;d.CH3CH2C≡CH.
;b.CH4; c.CH2=CHCH3;d.CH3CH2C≡CH. 查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中四种离子之间不可能满足:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| B、若满足:c(CH3COO-)=c(Na+),则该溶液一定呈中性 |
| C、若溶液中的溶质仅为CH3COONa,则离子间一定满足:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、若溶液中的溶质为CH3COONa和CH3COOH,则溶液中离子间可能满足:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
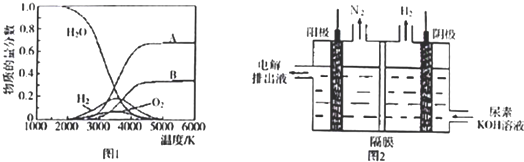
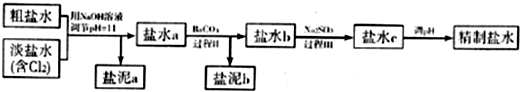
查看答案和解析>>
科目:高中化学 来源: 题型:
A、遇Fe(CN)
| ||||
B、水电离出c(OH-)>10-5mol?L-1;Mg2+、Cl-、NO
| ||||
C、遇石蕊变红的溶液:Na+、NH
| ||||
D、与铝反应产生大量氢气的溶液:Ba2+、HCO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 已知 | 类推 | |||||||||
| A | 将Fe加入CuSO4溶液中:Fe+Cu2+=Cu+Fe2+ | 将Na加入到CuSO4溶液中:2Na+Cu2+=Cu+2Na+ | ||||||||
| B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性:2H++SO42-+Ba++2OH-=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性:2H++SO42-+Ba++2OH-=BaSO4↓+2H2O | ||||||||
| C | 铁和氯气反应2Fe+3Cl2
|
铁和单质反应2Fe+3I2
| ||||||||
| D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染.
在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染.
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×10-4mol?L-1) |
10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×10-3mol?L-1) |
3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com