
【题目】如图所示,在铜锌原电池中,以稀硫酸为电解质溶液: 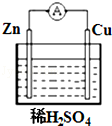
(1)锌片为极,电极上发生反应.(“氧化”或“还原”)
(2)电极反应式:
(3)锌片上观察到的现象:
(4)铜片为极,电极上发生反应.(“氧化”或“还原”)
(5)电极反应式:
(6)铜片上观察到的现象: .
【答案】
(1)负;氧化
(2)Zn﹣2e﹣=Zn2+
(3)Zn片溶解
(4)正;还原
(5)2H++2e﹣=H2↑
(6)有气泡生成
【解析】解:(1)铜锌原电池中,较为活泼的金属锌为原电池的负极,失去电子发生氧化反应,所以答案是:负;氧化;(2)较为活泼的金属锌为原电池的负极,失去电子发生氧化反应,电极反应式为Zn﹣2e﹣=Zn2+ , 所以答案是:Zn﹣2e﹣=Zn2+;(3)较为活泼的金属锌为原电池的负极,失去电子发生氧化反应,锌片上观察到的现象为锌逐渐溶解;所以答案是:Zn片溶解;(4)铜锌原电池中,正极为较不活泼的铜,发生还原反应,所以答案是:正;还原;(5)铜锌原电池中,正极为较不活泼的铜,氢离子在正极上得电子生成氢气,电极反应为,2H++2e﹣=H2↑,所以答案是:2H++2e﹣=H2↑;(6)氢离子在正极上得电子生成氢气,则铜片上观察到的现象是有气泡生成,所以答案是:有气泡生成.


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】三氧化铬(CrO3)常用于金属镀铬。工业上制造三氧化铬的化学方程式为:X+H2SO4=2CrO3+Na2SO4+H2O,其中X的化学式是
A. Na2CrO4 B. Na2Cr2O7 C. Na2Cr2O4 D. Na2CrO7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 1.8 g D2O含有NA个中子
B. 标准状况下,22.4 L己烷中共价键数目为19NA
C. 5.35 g NH4Cl固体中含有N—H键的个数为0.4NA
D. 常温下将0.1 mol Fe投入足量的浓硝酸中,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①蛋白质 ②油脂 ③葡萄糖 ④纤维素四种物质中,不能水解的是____(填序号),在人体中不能直接被消化吸收的是_________(填序号),蛋白质水解后生成_________(填名称,下同),油脂水解后生成___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应∶2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2;②单位时间内生成n molO2 的同时,生成2n mol NO;③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态;④混合气体的颜色不再改变的状态;⑤混合气体的密度不再改变的状态;⑥ 混合气体的平均相对分子质量不再改变的状态
A. ①④⑥ B. ②③⑤ C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_____________________。
(2)反应开始至2 min,气体Z的平均反应速率为______________。
(3)若X、Y、Z均为气体,反应达到平衡时:

①压强是开始时的_________倍;
②若此时将容器的体积缩小为原来的![]() 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为_______反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为_______反应(填“放热”或“吸热”)。
(4)若上述反应在2 min后的t1~t6内反应速率与反应时间图象如下,在每一时刻均改变一个影响反应速率的因素,则(_____)
A.在t1时增大了压强
B.在t3时加入了催化剂
C.在t4时降低了温度
D. t2~t3时X的转化率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两种试剂不能做喷泉实验的是( )
A. NO2 水 B. CO2 4 molL-1NaOH溶液
C. Cl2 饱和NaCl溶液 D. NH3 1 molL-1盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、[Al(OH)4]-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是( )

A. 原溶液中一定含有的阴离子是OH-、SiO32-、[Al(OH)4]-、CO32-
B. 反应后最终溶液中的溶质只有AlCl3
C. 原溶液中一定含有Na2SO4
D. 原溶液中含有CO32-与[Al(OH)4]-的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于离子反应,同时又属于有颜色变化的氧化还原反应的是( )
A. 氢气和氯气混合点燃
B. 氯化钡溶液和硫酸溶液混合
C. 把铜放入硫酸汞溶液中
D. 氯化铁溶液与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com