
分析 (1)Cl的质子数为17,原子结构中有3个电子层,最外层电子数为7;
(2)①根据化合物中总化合价为0计算出优氯净 Cl2Na(NCO)3中Cl元素的化合价;
②次氯酸具有强氧化性,能够与亚硫酸根离子发生氧化还原反应.
解答 解:(1)Cl的质子数为17,原子结构中有3个电子层,最外层电子数为7,则Cl元素位于周期表第三周期、ⅦA族,故答案为:第三周期、ⅦA族;
(2):①优氯净Cl2Na(NCO)3中,钠离子的化合价为+1价,N为-3价、O为-2价、C为+4价,设Cl元素的化合价为x,则:2x+(+1)+3[(-3)+(+4)+(-2)]=0,解得:x=+1,故答案为:+1;
②内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去,亚硫酸根离子与次氯酸反应生成硫酸钠和氯化氢或硫酸氢钠和盐酸,反应的化学方程式为:Na2SO3+HClO═Na2SO4+HCl,反应的离子方程式为:SO32-+HClO=SO42-+Cl-+H+,
故答案为:SO32-+HClO=SO42-+Cl-+H+.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应等为解答的关键,侧重分析与应用能力的考查,注意氯水的成分,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 单质沸点随原子序数的递增而升高 | |
| B. | 周期表第一列是第ⅠA 族元素,又称碱金属元素 | |
| C. | 金属锂常用于制造锂电池,这跟它还原性强、密度小有关 | |
| D. | 金属锂在空气中燃烧,产物是 Li2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
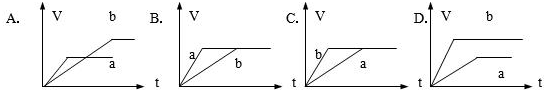
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
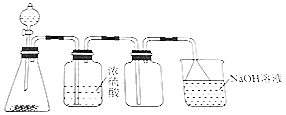 实验室需要制备、干燥和收集:①CO2、②Cl2、③SO2、④O2、⑤NO、⑥NO2、⑦H2、⑧NH3,其中能用如图所示装置进行实验的是( )
实验室需要制备、干燥和收集:①CO2、②Cl2、③SO2、④O2、⑤NO、⑥NO2、⑦H2、⑧NH3,其中能用如图所示装置进行实验的是( )| A. | ①②③④⑥ | B. | ⑤⑦⑧ | C. | ①②③④⑤⑥ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第6周期,第ⅣA族 | B. | 第7周期,第ⅥA族 | C. | 第7周期,第ⅣA族 | D. | 第8周期,第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠露置在空气中,光亮表面颜色变暗:4Na+O2═2Na2O | |
| B. | 铝条插入烧碱溶液中,开始没有明显现象:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 硫酸铵溶液与氢氧化钡溶液混合,产生气体:NH4++OH-═NH3↑十+H2O | |
| D. | 碘化银悬浊液滴加硫化钠溶液,黄色沉淀变成黑色:2AgI+S2-═Ag2S↓+2I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 作为催化剂的材料 | B. | 电子工业上的半导体材料 | ||
| C. | 制造农药的材料 | D. | 制造耐高温材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a | ||||||||||||||||||
| g | j | |||||||||||||||||
| b | c | f | i | l | m | |||||||||||||
| e | h | k | ||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com