
在300 ℃时,改变起始反应物中n(H2)对反应N2(g)+3H2(g)2NH3(g) ΔH<0的影响如图所示,下列说法正确的是( )
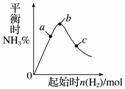
A.反应在b点达到平衡
B.b点H2的转化率最高
C.c点N2的转化率最高
D.a、b、c三点的平衡常数Kb>Ka>Kc
科目:高中化学 来源: 题型:
如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持及加热仪器已略)。
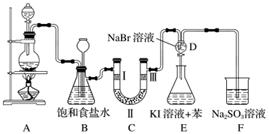
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关反应的化学方程式为__________________________。
装置B中饱和食盐水的作用是____________________。
同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:______________________________________________________________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入的物质为________(填字母)
| 选项 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入少量氯气时,可以看到无色溶液逐淅
变为________色,说明氯的非金属性大于溴。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是______________________________________________。
(4)装置F中用足量的Na2SO3溶液吸收多余氯气,试写出相应反应的离子方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于N2(g)+3H2(g)2NH3(g) K1
2NH3(g)N2(g)+3H2(g) K2
试分别写出平衡常数表达式,并判断其关系_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
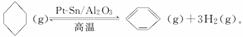 在某温度下,向恒容密闭容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=________。
在某温度下,向恒容密闭容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应的平衡常数与温度的关系如下表:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4的反应为放热反应
B.25 ℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80 ℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol·L-1,则此时v正>v逆
D.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.同族元素,随着电子层数的增加,I1逐渐增大
B.同周期元素,随着核电荷数的增加,I1逐渐增大
C.通常情况下,电离能I1<I2<I3
D.电离能越小,元素的金属性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组元素,按原子半径依次减小,元素第一电离能逐渐升高的顺序排列的是( )
A.K、Na、Li B.Al、Mg、Na
C.N、O、C D.Cl、S、P
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com