
| A. | NH4C1固体和Ba(OH)2晶体在常温下混合即可反应,是因为该反应是放热反应 | |
| B. | CO(g)的燃烧热是-283.0 KJ/mol,则 2CO2(g)═2CO(g)+O2(g)的反应热 为△H=+566.0 KJ/mol | |
| C. | 含1 mol Ba(OH)2的溶液和含1 mol H2SO4的溶液反应放出的热量是中和热 | |
| D. | 1 mol CH4燃烧生成水蒸气和二氧化碳所放出的热量是甲烷的燃烧热 |
分析 A.NH4Cl 固体和Ba(OH)2晶体在常温下的反应为吸热反应;
B.根据燃烧热计算;
C.反应还存在硫酸根离子和钡离子反应的反应热;
D.燃烧热指生产稳定氧化物时放出的热量.
解答 解:A.NH4Cl 固体和Ba(OH)2晶体在常温下的反应为吸热反应,故A错误;
B.CO(g)的燃烧热是283.0kJ/mol,则相同条件下2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol,分解时吸热,反应的热化学方程式为2CO2(g)=2CO(g)+O2(g)的△H=+566.0kJ/mol,故B正确;
C.H2SO4和Ba(OH)2反应的反应热包括中和反应和硫酸根离子和钡离子反应的反应热,故C错误;
D.燃烧热指生产稳定氧化物时放出的热量,生成水蒸气不是液态,故D错误.
故选B.
点评 本题较为综合,涉及中和热、燃烧热、学反应的能量变化特征应用、反应条件的分析判断,题目难度不大,注意把握相关概念.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:实验题
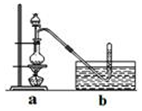 CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为-24.2℃,不易溶于水,易溶于乙醇和丙醇等有机溶剂.
CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为-24.2℃,不易溶于水,易溶于乙醇和丙醇等有机溶剂.| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.90 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )| A. | X、Y对应的氧化物都是酸性氧化物 | |
| B. | 最高价氧化物对应水化物的酸性W比Z弱 | |
| C. | Z比Y更容易与氢气化合 | |
| D. | W、Z对应的最高价氧化物对应的水化物的相对分子质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,-C15H27为链烃基,则漆酚不应具有的化学性质是( )
,-C15H27为链烃基,则漆酚不应具有的化学性质是( )| A. | 可以跟FeCl3溶液发生显色反应 | B. | 可以使酸性KMnO4溶液褪色 | ||
| C. | 可以跟Na2CO3溶液反应放出CO2 | D. | 可以发生取代反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
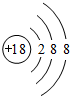 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②③⑤ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
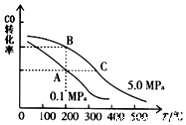 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com