
Č¼ĮĻµē³ŲŹĒČ¼ĮĻ(ĄżČēCO”¢H2”¢CH4µČ)øśŃõĘų»ņæÕĘų·“Ó¦£¬½«“Ė·“Ó¦µÄ»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆ£¬µē½āÖŹĶس£ŹĒKOHČÜŅŗ”£ŌņĻĀĮŠ¹ŲÓŚ¼×ĶéČ¼ĮĻµē³ŲµÄĖµ·ØÕżČ·µÄŹĒ(””””)
A£®øŗ¼«·“Ó¦Ź½ĪŖ£ŗCH4£«10OH£”Ŗ”śCO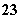 £«7H2O£«8e£
£«7H2O£«8e£
B£®øŗ¼«·“Ó¦Ź½ĪŖ£ŗO2£«2H2O£«4e£”Ŗ”ś4OH£
C£®Ėę×Å·“Ó¦½ųŠŠ£¬µē½āÖŹČÜŅŗ¼īŠŌ²»±ä
D£®øƵē³ŲµÄ×Ü·“Ó¦Óė¼×ĶéČ¼Éյķ“Ó¦·½³ĢŹ½ĻąĶ¬£¬·“Ó¦Ź½ĪŖ£ŗCH4£«2O2===CO2£«2H2O
“š°ø””A
½āĪö””±¾Ģāæ¼²éČ¼ĮĻµē³ŲµÄ·“Ó¦ŌĄķ”¢µē¼«·“Ó¦Ź½µÄŹéŠ“µČÖŖŹ¶”£¶ŌÓŚøĆČ¼ĮĻµē³Ų£¬øŗ¼«CH4Ź§µē×Ó±»Ńõ»Æ£¬ĘäÖŠ²śĪļÖ®Ņ»Ó¦ŹĒCO2£¬µ«ŌŚKOHČÜŅŗÖŠ£¬Ņ»¶Ø»į±äĪŖCO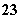 ”£¹Źµē¼«·“Ó¦ĪŖ£ŗCH4£«10OH£”Ŗ”śCO
”£¹Źµē¼«·“Ó¦ĪŖ£ŗCH4£«10OH£”Ŗ”śCO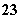 £«7H2O£«8e££»Õż¼«O2µĆµē×Ó±»»¹Ō£¬Éś³ÉĪļÓ¦Óėµē³ŲÖŠµē½āÖŹČÜŅŗĻą¹Ų”£µē¼«·“Ó¦ĪŖ£ŗO2£«2H2O£«4e£”Ŗ”ś4OH££»½«Į½øöµē¼«·“Ó¦Ź½Ļą¼Ó£¬¼“æɵƵ½×Ü·“Ó¦Ź½ĪŖ£ŗCH4£«2OH££«2O2===CO
£«7H2O£«8e££»Õż¼«O2µĆµē×Ó±»»¹Ō£¬Éś³ÉĪļÓ¦Óėµē³ŲÖŠµē½āÖŹČÜŅŗĻą¹Ų”£µē¼«·“Ó¦ĪŖ£ŗO2£«2H2O£«4e£”Ŗ”ś4OH££»½«Į½øöµē¼«·“Ó¦Ź½Ļą¼Ó£¬¼“æɵƵ½×Ü·“Ó¦Ź½ĪŖ£ŗCH4£«2OH££«2O2===CO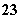 £«3H2O”£æɼūĖę×Å·“Ó¦µÄ½ųŠŠ£¬µē½āÖŹČÜŅŗÖŠc(OH£)²»¶Ļ¼õŠ””£
£«3H2O”£æɼūĖę×Å·“Ó¦µÄ½ųŠŠ£¬µē½āÖŹČÜŅŗÖŠc(OH£)²»¶Ļ¼õŠ””£


 ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
298 KŹ±£¬ø÷·“Ó¦µÄĘ½ŗā³£ŹżČēĻĀ£ŗ
¢ŁN2(g)£«O2(g)
 2NO(g)£¬K£½1”Į10£30£»
2NO(g)£¬K£½1”Į10£30£»
¢Ś2H2(g)£«O2(g)
 2H2O(g)£¬
2H2O(g)£¬
K£½2”Į1081 mol£1”¤L£»
¢Ū2CO2(g)
 2CO(g)£«O2(g)£¬K£½4”Į10£92 mol”¤L£1
2CO(g)£«O2(g)£¬K£½4”Į10£92 mol”¤L£1
Ōņ³£ĪĀĻĀ£¬NO”¢H2O”¢CO2ÕāČżÖÖ»ÆŗĻĪļ·Ö½ā·ÅŃõµÄĒćĻņ×ī“óµÄŹĒ(””””)
A£®¢Ł B£®¢Ś C£®¢Ū D£®ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¾ŪĀČŅŅĻ©ŹĒÉś»īÖŠ³£ÓƵÄĖÜĮĻ”£¹¤ŅµÉś²ś¾ŪĀČŅŅĻ©µÄŅ»ÖÖ¹¤ŅÕĀ·ĻßČēĻĀ£ŗ

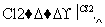 1£¬2¶žĀČŅŅĶé
1£¬2¶žĀČŅŅĶé

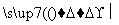 ¾ŪĀČŅŅĻ©
¾ŪĀČŅŅĻ©
·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ĪŖ__________________________________________£¬
·“Ó¦ĄąŠĶĪŖ__________________£¬·“Ó¦¢ŚµÄ·“Ó¦ĄąŠĶĪŖ______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ£ŗR—CH===CH2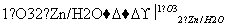 R—CHO£«HCHO
R—CHO£«HCHO
ŹŌŠ“³öŅŌ ĪŖÖ÷ŅŖŌĮĻÖʱø
ĪŖÖ÷ŅŖŌĮĻÖʱø µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼(ĪŽ»śŹŌ¼ĮČĪÓĆ)”£
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼(ĪŽ»śŹŌ¼ĮČĪÓĆ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¶Ō¼īŠŌŠæĆĢµē³ŲµÄŠšŹö²»ÕżČ·µÄŹĒ(””””)
A£®ZnŹĒÕż¼«£¬MnO2ŹĒøŗ¼«
B£®µē½āÖŹŹĒKOHČÜŅŗ
C£®Zn·¢ÉśŃõ»Æ·“Ó¦£¬MnO2·¢Éś»¹Ō·“Ó¦
D£®ĖüµÄÄÜĮæŗĶ“¢“ꏱ¼ä±ČĘÕĶØŠæĆĢµē³Ųøß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
±“ŵõ„ŹĒÓÉ°¢Ė¾Ę„ĮÖ”¢ĘĖČČĻ¢Ķ“¾»Æѧ·ØĘ“ŗĻÖʱøµÄ½āČČÕņĶ“æ¹Ń×Ņ©£¬ĘäŗĻ³É·“Ó¦Ź½ (·“Ó¦Ģõ¼žĀŌČ„)ČēĻĀ:

ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A. FeCl3ČÜŅŗæÉĒų±š°¢Ė¾Ę„ĮÖŗĶĘĖČČĻ¢Ķ“
B.1 mol±“ŵõ„×ī¶ąæÉĻūŗÄ3 mol NaOH
C.³£ĪĀĻĀ£¬±“ŵõ„ŌŚĖ®ÖŠµÄČܽā¶ČŠ”ÓŚĘĖČČĻ¢Ķ“
D.Óė°¢Ė¾Ę„ĮÖ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬ĒŅ1 molÄÜÓė×ć×īNaHCO3ČÜŅŗ·“Ó¦²śÉś2mo1CO2µÄ½į¹¹ĪŖ10ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠ»śĪļAµÄ²śĮæŹĒŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ¹¤Ņµ·¢Õ¹Ė®Ę½µÄ±źÖ¾£¬æÉ·¢ÉśŅŌĻĀĻµĮŠ×Ŗ»Æ£¬B”¢DŹĒÉś»īÖŠ³£¼ūµÄĮ½ÖÖÓŠ»śĪļ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
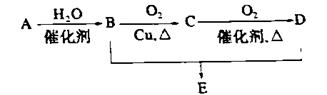
A.AµÄ½į¹¹¼ņŹ½ĪŖCH2= CH2
B.1mol BĪļÖŹæÉŅŌÓė×ćĮæNa·“Ӧɜ³É0.5mol H2
C.B”¢D”¢EČżÖÖĪļÖŹæÉŅŌÓƱ„ŗĶNa2CO3ČÜŅŗ¼ų±š
D.ÓÉB”¢DÖʱøEÅØH2SO4Ö»×÷ĪüĖ®¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŅ»¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ×ÅČēĻĀ·“Ó¦£ŗ
CO2(g) + H2(g)  CO(g) + H2O(g)
CO(g) + H2O(g)
ĘäĘ½ŗā³£Źż£ĖŗĶĪĀ¶ČtµÄ¹ŲĻµČēĻĀ£ŗ
| t”ę | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1) KµÄ±ķ“ļŹ½ĪŖ£ŗ”” ””£»
(2) øĆ·“Ó¦µÄÕż·“Ó¦ĪŖ”””” ””·“Ó¦£Ø”°ĪüČČ”±»ņ”°·ÅČČ”±£©
(3) ÄÜÅŠ¶ĻøĆ·“Ó¦ŹĒ·ńŅŃ¾“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ£ŗ
£Į£®ČŻĘ÷ÖŠŃ¹Ēæ²»±ä £Ā£®»ģŗĻĘųĢåÖŠCOÅØ¶Č²»±ä
£Ć£®v(H2)Õż = v(H2O)Äę D£®c(CO2) = c(CO)””
E£®ČŻĘ÷ÖŠĘųĢåĆÜ¶Č²»±ä F£®1mol H—H¼ü¶ĻĮѵÄĶ¬Ź±¶ĻĮŃ2 mol H-O¼ü
(4) ŌŚ850”ꏱ£¬æÉÄę·“Ó¦£ŗCO2(g) + H2(g)  CO(g) + H2O(g)£¬ŌŚøĆČŻĘ÷ÄŚø÷ĪļÖŹµÄÅØ¶Č±ä»ÆČēĻĀ£ŗ
CO(g) + H2O(g)£¬ŌŚøĆČŻĘ÷ÄŚø÷ĪļÖŹµÄÅØ¶Č±ä»ÆČēĻĀ£ŗ
| Ź±¼ä/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2 O ( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
3min—4min“ļµ½Ę½ŗāŹ±COµÄĘ½ŗāÅضČc3= £Øc3¾«Č·µ½Š”ŹżµćŗóĆęČżĪ»Źż£©£¬CO2 (g)µÄ×Ŗ»ÆĀŹ= ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
“Óŗ£“ųÖŠĢįČ”µāµÄŹµŃé¹ż³ĢÖŠ,Éę¼°ĻĀĮŠ²Ł×÷,ĘäÖŠÕżČ·µÄŹĒ(””””)
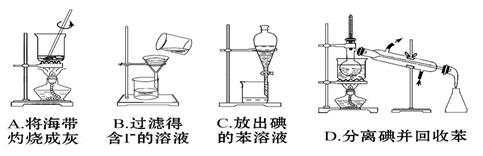
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com