
分析 镁、铝、铜合金中加入过量的盐酸充分反应,只有Cu不反应,剩余固体为铜,再向混合液中加入50mL 2mol-1的FeC13溶液恰能使剩余固体完全溶解,发生反应为Cu+2Fe3+=Cu2++2Fe2+,根据氯化铁的物质的量可计算出铜的质量,从而可知合金中镁和铝的质量,然后结合生成氢气的量列式计算,
(1)根据m=nM计算出合金中铜的质量;
(2)合金中只有Al与氢氧化钠溶液反应,结合电子守恒计算出生成氢气的物质的量,最高价V=nVm计算出氢气在标准状况下的体积.
解答 解:(1)镁、铝、铜合金中加入过量的盐酸充分反应,只有Cu不反应,剩余固体为铜,再向混合液中加入50mL 2mol-1的FeC13溶液恰能使剩余固体完全溶解,发生反应为Cu+2Fe3+=Cu2++2Fe2+,
50mL 2mol-1的FeC13溶液中含有Fe3+的物质的量为:2mol/L×0.05L=0.1mol,则n(Cu)=$\frac{1}{2}$n(Fe3+)=0.05mol,
所以合金中含有铜的质量为:64g/mol×0.05mol=3.2g,
故答案为:3.2g;
(2)合金中Mg、Al的质量为:7.1g-3.2g=3.9g,生成氢气的物质的量为:$\frac{4.48L}{22.4L/mol}$=0.2mol,
设合金中含有Mg、Al的物质的量分别为x、y,
则$\left\{\begin{array}{l}{24x+27y=3.9}\\{x+1.5y=0.2}\end{array}\right.$
解得:$\left\{\begin{array}{l}{x=0.05mol}\\{y=0.1mol}\end{array}\right.$,
若将此合金放入过量的烧碱溶液中,只有0.1molAl参与反应,根据电子守恒可知生成氢气的物质的量为:$\frac{0.1mol×3}{2}$=0.15mol,
标准状况下0.15mol氢气的体积为:22.4L/mol×0.15mol=3.36L,
故答案为:0.36L.
点评 本题考查了混合物反应的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题侧重考查学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,用0.1000mol•L-1的盐酸滴定0.1000mol•L-1Na2CO3溶液25.00mL.用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是( )
常温下,用0.1000mol•L-1的盐酸滴定0.1000mol•L-1Na2CO3溶液25.00mL.用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是( )| A. | c→d发生的主要离子反应:HCO3-+H+=H2O+CO2 | |
| B. | 在b点 时,c(CO32-)>c(HCO3)->c(OH-) | |
| C. | 在d点 时,c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| D. | 在e点 时c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 结论 |
| A | 向纯碱中滴加足量浓盐酸,将产生的气体通入硅酸钠溶液,溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
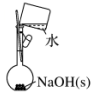
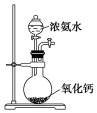
| A.配制0.10 mol•L-1 NaOH溶液 | B.制备少量氨气 |
 |  |
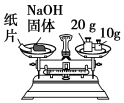
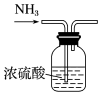
| C.称量氢氧化钠固体质量 | D.干燥氨气 |
 |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸水溶液的pH<7:H2SO3?2H++SO32- | |
| B. | 将亚硫酸滴入饱和Na2CO3溶液有气泡产生:2H++CO32-═H2O+CO2↑ | |
| C. | Na2SO3溶液能使红色石蕊变蓝:SO32-+H2O═HSO3-+OH- | |
| D. | Na2SO3溶液中加入足量的酸化Ba(NO3)2溶液出现白色沉淀:3SO32-+2NO3-+2H++3Ba2+═3BaSO4↓+2NO↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作和现象 | 实验结论 | |
| A | SO2通入Ba(NO3)2溶液中有白色沉淀生成 | 白色沉淀是BaSO3 |
| B | 向某待检液中滴加盐酸酸化的BaCl2溶液,生成白色沉淀 | 该待检液中可能不含有SO42- |
| C | 将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置,下层分别呈无色和紫红色 | 氧化性:Fe3+>Br2>I2 |
| D | 向浓度均为0.1mol/L的KCl、KI混合液中滴加1~2滴0.01mol/LAgNO3溶液,产生黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com