
| A£® | 0.1 mol/LµÄNaHAČÜŅŗpH=5£¬ŌņČÜŅŗ£ŗc£ØHA-£©£¾c£ØH+£©£¾c£ØA2-£©£¾c£ØH2A£© | |
| B£® | µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄNaCl£Øaq£© Ī¢Į£ÖÖĄą“óÓŚNaClO£Øaq£©ÖŠĪ¢Į£ÖÖĄą | |
| C£® | pH=3µÄĮņĖįČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č“óÓŚpH=11µÄ°±Ė®ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č | |
| D£® | Ģå»żĻąĶ¬µÄ0.1 mol/L°±Ė®ŗĶ0.1 mol/L NaOHČÜŅŗÖŠŗĶŃĪĖįµÄÄÜĮ¦ŗóÕß“ó |
·ÖĪö A£®ČÜŅŗĻŌŹ¾ĖįŠŌ£¬HA-µÄµēĄė³Ģ¶Č“óÓŚĖ®½ā³Ģ¶Č£¬Ōņc£ØA2-£©£¾c£ØH2A£©£¬ĒāĄė×Ó»¹Ą“×ŌĖ®µÄµēĄė£¬Ōņc£ØH+£©£¾c£ØA2-£©£»
B£®NaClČÜŅŗÖŠŗ¬ÓŠÄĘĄė×Ó”¢ĀČĄė×Ó”¢ĒāŃõøłĄė×Ó”¢ĒāĄė×ÓŗĶĖ®·Ö×Ó£¬×ܹ²ÓŠ5ÖÖ£¬“ĪĀČĖįÄĘČÜŅŗÖŠ“ęŌŚÄĘĄė×Ó”¢“ĪĀČĖįøłĄė×Ó”¢ÄĘĄė×Ó”¢ĒāĄė×Ó”¢ĒāŃõøłĄė×ÓŗĶĖ®·Ö×Ó£»
C£®ĮņĖįŗĶ°±Ė®¶¼ŅÖÖĘĮĖĮĖĖ®µÄµēĄė³Ģ¶Č£¬Į½ČÜŅŗÖŠĒāĄė×Ó”¢ĒāŃõøłĄė×ÓÅØ¶Č“óŠ”Ó°ĻģĖ®µÄµēĄė£»
D£®°±Ė®ŗĶĒāŃõ»ÆÄʵÄÅضČĻąĶ¬£¬µ±Ģå»żĻąĶ¬Ź±ĻūŗĵÄHClµÄĪļÖŹµÄĮæĻąĶ¬£®
½ā“š ½ā£ŗA.0.1 mol/LµÄNaHAČÜŅŗpH=5£¬ĖµĆ÷HA-µÄµēĄė³Ģ¶Č“óÓŚĖ®½ā³Ģ¶Č£¬ČÜŅŗĻŌŹ¾ĖįŠŌ£¬ĖłŅŌĄė×ӓ󊔹ŲĻµŹĒ£ŗc£ØHA-£©£¾c£ØH+£©£¾c£ØA2-£©£¾c£ØH2A£©£¬¹ŹAÕżČ·£»
B£®NaClČÜŅŗÖŠŗ¬ÓŠÄĘĄė×Ó”¢ĀČĄė×Ó”¢ĒāŃõøłĄė×Ó”¢ĒāĄė×ÓŗĶĖ®·Ö×Ó£¬×ܹ²ÓŠ5ÖÖĄė×Ó£¬NaClOČÜŅŗÖŠ“ęŌŚÄĘĄė×Ó”¢“ĪĀČĖįøłĄė×Ó”¢ÄĘĄė×Ó”¢ĒāĄė×Ó”¢ĒāŃõøłĄė×ÓŗĶĖ®·Ö×Ó£¬×ܹ²ŗ¬ÓŠ6ÖÖĄė×Ó£¬ĖłŅŌNaClČÜŅŗÖŠµÄĪ¢Į£ÖÖĄąŠ”ÓŚNaClOČÜŅŗ£¬¹ŹB“ķĪó£»
C£®pH=3µÄĮņĖįČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ0.001mol/L£¬pH=11µÄ°±Ė®ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČĪŖ0.001mol/L£¬Į½ČÜŅŗ¶¼ŅÖÖĘĮĖĖ®µÄµēĄė£¬ÓÉÓŚĮņĖįÖŠĒāĄė×ÓÓė°±Ė®ÖŠĒāŃõøłĄė×ÓÅضČĻąµČ£¬ŌņĮ½ČÜŅŗ¶ŌĖ®µÄµēĄė³Ģ¶ČÓ°ĻģĻąĶ¬£¬¹ŹC“ķĪó£»
D£®Ģå»żĻąĶ¬µÄ0.1 mol/L°±Ė®ŗĶ0.1 mol/L NaOHČÜŅŗÖŠŗ¬ÓŠČÜÖŹµÄĪļÖŹµÄĮæĻąĶ¬£¬ŌņĮ½ČÜŅŗÖŠŗĶŃĪĖįµÄÄÜĮ¦ĻąĶ¬£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖĄė×ÓÅØ¶Č“óŠ”±Č½Ļ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ŃĪµÄĖ®½āŌĄķ¼°ĘäÓ°ĻģĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕÅŠ¶ĻĄė×ÓÅØ¶Č“óŠ”µÄ³£ÓĆ·½·Ø£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2 | B£® | N2 | ||
| C£® | NO2 | D£® | Ö±¾¶·Ē³£Š”µÄæÉĪüČėæÅĮ£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HClĖ®ČÜŅŗŹĒĒæĖį£¬ČĪŗĪĒæĖį¶¼µ¼ÖĀÓŠ³ĮµķĪö³ö | |
| B£® | Cl-ÅضČŌö“ó£¬Ź¹Ę½ŗāĻņÉś³ÉĀČ»ÆÄʵķ½ĻņŅĘ¶Æ£¬Éś³ÉNaCl£Øs£© | |
| C£® | ĖįµÄ“ęŌŚ½µµĶĮĖKsp£ØNaCl£©µÄŹżÖµ | |
| D£® | Ksp£ØNaCl£©²»ŹÜĖįµÄÓ°Ļģ£¬µ«Ōö¼ÓCl-ÅØ¶Č£¬ÄÜŹ¹Ksp£ØNaCl£©¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃéŹŅÓĆÉÕ¼īČÜŅŗ³żČ„Ī²ĘųÖŠµÄCl2£ŗCl2+OH-ØTCl-+HClO | |
| B£® | Ļ”ĻõĖįÖŠ¼ÓČė¹żĮæĢś·Ū£ŗFe+4H++NO3-=Fe3++NO”ü+2H2O | |
| C£® | ŹÆ»ŅĖ®ÖŠ¼ÓČė¹żĮ抔ĖÕ“ņČÜŅŗ£ŗ2HCO3-+Ca2++2OH-=CaCO3”ż+CO32+2H2O | |
| D£® | ĻņNaAlO2ČÜŅŗÖŠĶØČė¹żĮæCO2£ŗ2AlO2-+CO2+3H2O”ś2Al£ØOH£©3”ż+CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ³ĮµķĪļ | æŖŹ¼³Įµķ | ĶźČ«³Įµķ |
| Al£ØOH£©3 | 3.8 | 5.2 |
| Fe£ØOH£©3 | 2.7 | 3.2 |
| Fe£ØOH£©2 | 7.6 | 9.7 |
| Ni£ØOH£©2 | 7.1 | 9.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C1=C2 | B£® | C1£¾C2 | C£® | C1£¼C2 | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃé½įŹųŗó½«ĖłÓŠµÄ·ĻŅŗµ¹ČėĻĀĖ®µĄÅųöŹµŃéŹŅ£¬ŅŌĆāĪŪČ¾ŹµŃéŹŅ | |
| B£® | ĪŖĮĖŹ¹Ńų·Ö»¹Ģļ¶ų½«Ö²Īļ½ÕøŃ·ŁÉÕ“¦Ąķ | |
| C£® | PM2.5ŹĒÖø“óĘųÖŠÖ±¾¶½Ó½üÓŚ2.5”Į10-6m£Ø1m=109nm£©µÄæÅĮ£Īļ£¬ÕāŠ©ĻøæÅĮ£Īļ·ÖÉ¢ŌŚæÕĘųÖŠŠĪ³ÉµÄ·ÖÉ¢ĻµŹĒ½ŗĢå | |
| D£® | ŹµĻÖ׏Ō“µÄ”°3R”±ĄūÓĆ£¬¼“£ŗ¼õɣ׏Ō“ĻūŗÄ£ØReduce£©”¢Ōö¼Ó׏Ō“µÄÖŲø“Ź¹ÓĆ£ØReuse£©”¢Ģįøß׏Ō“µÄŃ»·ĄūÓĆ£ØRecycle£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
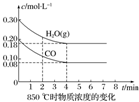 ŅŃÖŖ£ŗCO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©”÷H=Q£¬ĘäĘ½ŗā³£ŹżĖęĪĀ¶Č±ä»ÆČēĻĀ±ķĖłŹ¾£ŗ
ŅŃÖŖ£ŗCO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2£Øg£©”÷H=Q£¬ĘäĘ½ŗā³£ŹżĖęĪĀ¶Č±ä»ÆČēĻĀ±ķĖłŹ¾£ŗ| ĪĀ¶Č/”ę | 400 | 500 | 850 |
| Ę½ŗā³£Źż | 9.94 | 9 | 1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com