
【题目】已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体。反应生成的水均已略去。它们有如下图所示的关系。
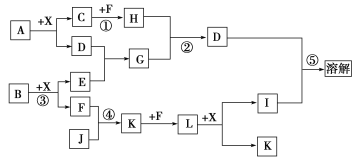
(1)写出化学式:A________,B________,J________;
(2)反应③中每生成1 mol F,转移电子的数目为______________;
(3)反应④的化学方程式为:______________________________;
(4)写出离子方程式:反应②________________________________,反应⑤________________________________________________。
【答案】Al4C3 Na2O2 NH3 2NA 4NH3+5O2![]() 4NO+6H2O 2AlO2-+CO2+3H2O=Al(OH)3↓+CO32-(CO2少量)或者AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(CO2过量) Al(OH)3+3H+=Al3++3H2O
4NO+6H2O 2AlO2-+CO2+3H2O=Al(OH)3↓+CO32-(CO2少量)或者AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(CO2过量) Al(OH)3+3H+=Al3++3H2O
【解析】
B是一种淡黄色固体,即B是Na2O2,能与过氧化钠反应的物质为CO2和H2O,X为常见的无色液体,即X为H2O,过氧化钠与H2O反应生成NaOH和O2,C是含氢量最高的烃,即C为CH4,C、J是同周期元素的气态氢化物,即J为NH3,E为NaOH,F为O2,K为NO,L为NO2,I为HNO3,反应⑤后是溶解,则D为溶于硝酸的沉淀,反应①为甲烷的燃烧,即H为CO2,能与NaOH反应生成沉淀,大胆猜测为Al(OH)3,则G为NaAlO2,CO2能与AlO2-反应生成Al(OH)3,根据元素守恒,推出A中含有的元素为Al和C,A的化学式为Al4C3,其中Al元素质量分数为75%,C的质量分数为25%,符合题意,据此分析。
(1)根据上述分析,A为Al4C3,B为Na2O2,J为NH3;
(2)反应③为2Na2O2+2H2O=4NaOH+O2↑,生成1molO2,转移电子物质的量为2mol,即转移电子数目为2NA;
(3)反应④为氨气的催化氧化,化学反应方程式为4NH4+5O2![]() 4NO+6H2O;
4NO+6H2O;
(4)反应②离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-(CO2少量)或者AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(CO2过量);反应⑤的离子方程式为Al(OH)3+3H+=Al3++3H2O。


 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.从1L1mol/L的氯化钠溶液中取出10mL,其浓度仍是1mol/L
B.制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况)
C.0.5L2mol/L的氯化钡溶液中,钡离子和氯离子总数为3×6.02×1023
D.10g98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的浓度是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度为0.1 mol·L-1、体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图中信息回答下列问题:

(1)该温度时NH3·H2O的电离常数K=________。
(2)滴定过程中所用盐酸的pH=________。
(3)比较b、c、d三点时的溶液中,由水电离出的c(OH-)大小顺序为___________。(填字母)
(4)滴定时,由b点到c点的过程中,下列各选项中数值变大的是___(填字母,下同)。
A.c(H+)·c(OH-) B. c(H+)·c(NH3·H2O)/c(NH4+)
C. c(NH4+)·c(OH-)/c(NH3·H2O) D. c(H+)/c(OH-)
(5)根据以上滴定曲线判断下列说法正确的是________(溶液中N元素只存在NH4+和NH3·H2O两种形式)。
A.点b所示溶液中:c(NH4+)+c(H+)=c(OH-)+c(NH3·H2O)
B.点c所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH4+)
C.点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.滴定过程中可能有:c(NH3·H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)
(6)d点之后若继续加入盐酸至图像中的e点(不考虑NH4+水解的影响),则e点对应的横坐标为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.从1L2mol·L-1的NaCl溶液中取出10mL,所得溶液的浓度是0.02mol·L-1
B.标准状况下22.4LHCl气体溶于1L水,所得溶液的浓度为1.00mol·L-1
C.98﹪(密度1.84g·cm-3)硫酸的物质的量浓度是18.4mol·L-1
D.10mL10.0mol·L-1 Na2SO4溶液加水90mL,所得溶液的浓度是1.00mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶无色澄清的溶液,溶质由NH4NO3、KCl、CuCl2、Ba(NO3)2、Na2CO3中的一种或几种配制而成。为了确定其中的溶质,用该溶液做如下实验:
①取少许溶液,加入足量的盐酸有气泡产生
②再向①的溶液中滴加硝酸银溶液有白色沉淀生成
③取原溶液少量,加入NaOH溶液并加热,产生刺激性气味的气体,并用湿润的红色石蕊试纸检验气体,试纸变蓝
(1)根据以上事实判断:肯定存在的溶质是___;肯定不存在的溶质是___;不能确定是否存在的溶质是___;设计实验证明是否存在该溶质:___。
(2)写出上述实验③中产生刺激性气味气体的反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Na表示阿伏加德罗常数的值,下列叙述错误的是
A.含有NA个氢原子的氢气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64gSO2中含有的原子数为3Na
C.在常温常压下,35.5g Cl2含有的分子数为0.5Na
D.标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)19g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,ACl2的摩尔质量是__________________,A的相对原子质量是______________。
(2)1.5mol CO2中含_____ mol碳原子,________个氧原子(以NA为阿伏加德罗常数的值),标准状况下的体积为___________L。
① 实验室利用石灰石制备CO2______________________________________________
② SO2和足量NaOH反应 __________________________________________________
③写一个置换反应方程式 ______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】伪麻黄碱(D)是新康泰克的成分之一,能够缓解感冒时带来的鼻塞、流鼻涕和打喷嚏等症状,其中一种合成路线如下:
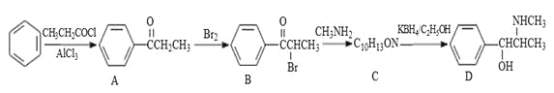
回答下列问题:
(1)伪麻黄碱(D)的分子式为 ;B中含有的官能团有 (写名称)。
(2)写出 B—C反应的化学方程式: 。C—D的反应类型为 。
(3)B的消去产物可以用于合成高分子化合物E,请写出 E的结构简式: 。
(4)满足下列要求的A的同分异构体有 种;
①能发生银镜反应
②苯环上的一氯代物有两种结构,其中核磁共振氢谱为4组峰,且峰面积之比为6:2:1:1的为 (写结构简式)。
(5)已知:![]() 。参照上述合成路线,设计一条由苯和乙酸为起始原料制备
。参照上述合成路线,设计一条由苯和乙酸为起始原料制备![]() 的合成路线: 。
的合成路线: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于氧化还原反应的是( )
A.3Cl2+6KOH=5KCl+KClO3+3H2OB.Ca(OH)2+CO2=CaCO3↓+H2O
C.Cl2+H2O ![]() HCl+HClOD.5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O
HCl+HClOD.5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com