
下列说法正确的是( )
A.
图中△H1=△H2+△H3
B.
如图在催化剂条件下,反应的活化能等于E1+E2
C.
如图表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线
D.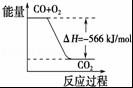
如图可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年安徽六安市高二下第三次月考化学试卷(解析版) 题型:选择题
某烃的结构简式为: ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,一定在同一平面上的碳原子数为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,一定在同一平面上的碳原子数为c,则a、b、c分别为( )
A.4,3,5 B.4,3,6 C.2,5,4 D.4,6,4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期6月月考化学试卷(解析版) 题型:推断题
过渡金属催化的新型碳碳偶联反应是近年来有机合成的研究热点之一,如:
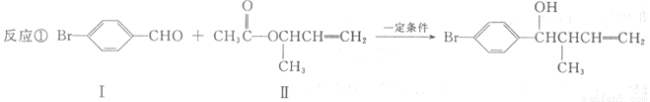
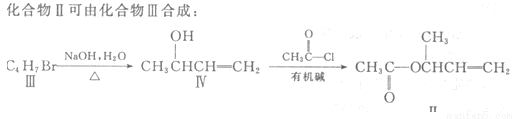
(1)化合物I的分子式为 。
(2)化合物Ⅱ与Br2加成的产物的结构简式为 。
(3)化合物Ⅲ的结构简式为 。
(4)在浓硫酸存在和加热条件下,化合物Ⅳ易发生消去反应生成不含甲基的产物,该反应方程式为 因此,在碱性条件下,由Ⅳ与CH3CO--Cl反应合成Ⅱ,其反应类型为 。
(5)Ⅳ的一种同分异构体V能发生银镜反应。V与Ⅱ也可发生类似反应①的反应,生成化合物Ⅵ,Ⅵ的结构简式为 (写出其中一种)。
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上第四次质检化学试卷(解析版) 题型:实验题
合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义.以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图.

(1)本工艺中所用的原料除CaSO4•2H2O、KCl外,还需要 等原料
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有 (填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO32﹣的方法是: .
(5)已知不同温度下K2SO4在100g水中达到饱和时溶解的量如下表:
温度(℃) | 0 | 20 | 60 |
K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
60℃时K2SO4的饱和溶液591g冷却到0℃,可析出K2SO4晶体 g
(6)氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是
A、熔点较低 b、能导电 c、能制冷 d、无毒
(7)上述工艺流程中体现绿色化学理念的是: .
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上第四次质检化学试卷(解析版) 题型:选择题
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有( )
A.15种 B.28种 C.32种 D.40种
查看答案和解析>>
科目:高中化学 来源:2016届广东省广州市高三下4月月考化学试卷(解析版) 题型:实验题
湖南盛产的山苍子油中柠檬醛含量很高,质量分数可达到60%﹣90%,柠檬醛也可以利用异戊二烯为原料人工合成,柠檬醛又可用来成紫罗兰酮等香精香料,其合成路线如下:

已知:
① +Cl2
+Cl2
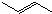
②
③同一碳原子连有两个双键结构不稳定.
试根据上述转化关系回答下列问题:
(1)写出A的结构简式 ,C的结构简式 .
(2)①对应的反应条件是 ,反应③的反应类型是 .
(3)写出B转化为柠檬醛的化学方程式 .
(4)根据反应②的反应机理写出CH3CHO与足量的HCHO反应产物的结构简式: .
(5)检验柠檬醛中含有碳碳双键的实验方法是: .
(6)α﹣紫罗兰酮、β﹣紫罗兰酮有很多同分异构体,则满足下列条件的同分异构体有 种.
①含有一个苯环
②属于醇类且不能发生催化氧化反应
③核磁共振氢谱显示有5个峰.
查看答案和解析>>
科目:高中化学 来源:2016届广东省广州市高三下4月月考化学试卷(解析版) 题型:选择题
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g)△H=+Q kJ•mol﹣1(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol•L﹣1,则H2的反应速率为0.03 mol•(L•min﹣1)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol•L﹣1的NaOH溶液中恰好反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省运城市高二上学期单元测4化学试卷(解析版) 题型:填空题
溴化碘(IBr)的化学性质类似于卤素单质,试完成下列问题:
(1)溴化碘的电子式是 ,它是由 键形成的 分子.
(2)溴化碘和水反应生成了一种三原子分子,该分子的电子式为 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高一下第二次月考化学试卷(解析版) 题型:填空题
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.
(1)从能量的角度看,断开化学键要 (填“放出”或“吸收”)能量.已知拆开1molH﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、300kJ.则由H2和I2反应生成1mol HI需要 (填“放出”或“吸收”) kJ的热量.
(2)某兴趣小组为研究原电池原理,设计如图1装置:
①a和b用导线连接,Zn发生 (填“氧化”或“还原”)反应.其电极反应式为 .溶液H+移向 (填“Cu”或“Zn”)极.
②无论a和b是否连接,Zn片均被腐蚀.若转移了0.4mol电子,则理论上Zn片质量减轻 g.
(3)①目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是 (填序号).
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是 (填序号).
a.以上反应是可逆反应
b.充电时化学能转变为电能
c.放电时化学能转变为电能
②图2为氢氧燃料电池的构造示意图,根据电子运动方向可知,则X极为电池的 (填“正”或“负”)极,Y极的电极反应方程式为 .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com