
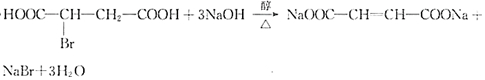 .
. 在该条件下,1mol N生成2mol I,N的结构简式是
在该条件下,1mol N生成2mol I,N的结构简式是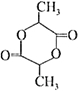 .
.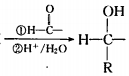 以苯和乙醛为原料制备H,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
以苯和乙醛为原料制备H,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):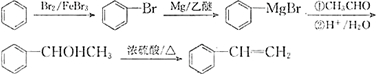 .
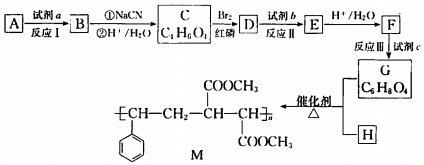
. 分析 烃A的相对分子质量为28,则A的结构简式为CH2=CH2,由已知:R-X$→_{②H+/H_{2}O}^{①NaCN}$R-COOH条件得,B中含卤素原子,故试剂a为Br2的CCl4,CH2=CH2与Br2的CCl4发生加成反应生成B,则B的结构简式为BrCH2-CH2Br,根据已知条件得C的结构简式为HOOC-CH2-CH2-COOH,由M可知H为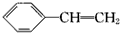 ,G为CH3OOC-CH=CH-COOCH3,则F为HOOC-CH=CH-COOH,由此可知C与Br2的红磷发生取代反应,D的结构简式为HOOC-CHBr-CH2-COOH,E为NaOOC-CH=CH-COONa,以此解答该题.
,G为CH3OOC-CH=CH-COOCH3,则F为HOOC-CH=CH-COOH,由此可知C与Br2的红磷发生取代反应,D的结构简式为HOOC-CHBr-CH2-COOH,E为NaOOC-CH=CH-COONa,以此解答该题.
解答 解:(1)由以上分析可知A为CH2=CH2,故答案为:CH2=CH2;
(2)a为Br2的CCl4溶液,故答案为:Br2/CCl4;
(3)由以上分析可知C为HOOC-CH2-CH2-COOH,故答案为:HOOC-CH2-CH2-COOH;
(4)反应II为HOOC-CHBr-CH2-COOH的消去反应,反应的化学方程式是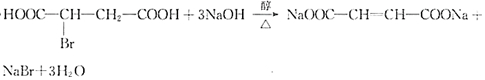 ,
,
故答案为: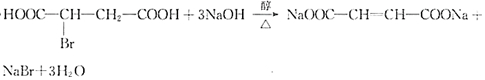 ;
;
(5)反应Ⅲ为HOOC-CH=CH-COOH与甲醇的酯化反应,也为取代反应,故答案为:酯化反应(取代反应);
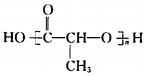
(6) 对应的单体I为CH3CHOHCOOH,1mol N生成2mol I,可知N为
对应的单体I为CH3CHOHCOOH,1mol N生成2mol I,可知N为 ,
,
故答案为: ;
;
(7)H为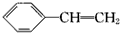 ,以苯和乙醛为原料制备H,可先由苯和溴在溴化铁作用下发生取代反应生成溴苯,溴苯与Mg/乙醚作用下生成
,以苯和乙醛为原料制备H,可先由苯和溴在溴化铁作用下发生取代反应生成溴苯,溴苯与Mg/乙醚作用下生成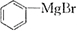 ,然后与乙醛反应生成
,然后与乙醛反应生成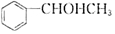 ,经消去反应可生成
,经消去反应可生成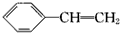 ,则反应的流程为
,则反应的流程为 ,
,
故答案为: .
.
点评 本题考查无机物的推断,为高频考点,侧重考查学生的分析能力,本题注意把握题给信息,为解答该题的关键,注意以乙烯为突破口,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钾与硫酸的反应 | B. | 锌与盐酸反应放出氢气 | ||
| C. | CO2通过炽热的焦炭发生的反应 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W的最高价氧化物能与水反应生成相应的酸 | |
| B. | 室温下,0.05mol•L-1的M的气态氢化物的水溶液的PH>l | |
| C. | 简单离子半径由大到小的顺序:Y>Z>M | |
| D. | Y、Z元素的单质作电极,在NaOH溶液环境下构成原电池,Z电极上产生大量气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
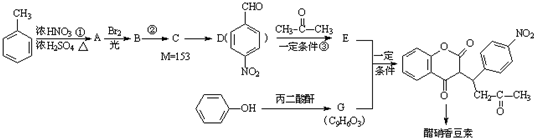

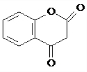 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| C(NO)/mol•L-1 | 9.50×10-3 | 4.50×10-3 | 2.50×10-5 | 1.50×10-3 | 1.5×10-3 |
| C(CO)/mol•L-1 | 9.00×10-3 | 4.00×10-3 | 2.00×10-3 | 1.00×10-3 | 1.00×10-3 |
| A. | -定温度下,从开始到平衡,该反应的平衡常数逐渐增大 | |
| B. | 前2s内的平均反应速率v(N2)=1.75×10-3 mol•L-1•s-1 | |
| C. | 达到平衡时,CO的转化率为11.11% | |
| D. | 3s时NO和CO的浓度都不再变化,反应停止进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3易液化,氨常用作制冷剂 | |
| B. | 胆矾遇浓硫酸变白是因为浓硫酸的脱水性 | |
| C. | 氨催化氧化制硝酸过程中的三个主要反应都属于氧化还原反应 | |
| D. | 浓硝酸需保存在棕色瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
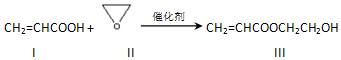
| A. | 化合物Ⅰ能与NaHCO3溶液反应生成CO2 | |
| B. | 可用Br2的CCl4溶液检验化合物Ⅲ中是否混有化合物I | |
| C. | 化合物Ⅱ与乙醛互为同分异构体 | |
| D. | 化合物Ⅲ水解可生成2种有机物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com