
【题目】物质有以下转化关系:

根据上图和实验现象,回答下列问题:(用化学式表示)
(1)A是_____,X粉末是_______;
(2)写出反应①的化学方程式___________________;
(3)写出反应②的离子方程式___________________;
(4)写出除去固体C中混有的NaHCO3的化学方程式____________。
【答案】Na2O2 Cu 2Na2O2+2CO2 = 2Na2CO3+O2 Cu2+ +2OH- = Cu(OH)2↓ ![]()
【解析】
淡黄色的粉末可以是单质硫或是过氧化钠,但是能和二氧化碳反应的淡黄色粉末只有过氧化钠,则气体B为氧气,固体C为碳酸钠;X粉末与氧气加热反应生成黑色固体,黑色固体与硫酸反应得蓝色溶液,则X为Cu;蓝色溶液为硫酸铜溶液;碳酸钠与澄清石灰水反应得到NaOH溶液,NaOH与硫酸铜溶液反应得到氢氧化铜蓝色沉淀。
(1)能和二氧化碳反应的淡黄色粉末只有过氧化钠,即A为![]() ,蓝色溶液是含有铜离子的溶液,结合上述分析,X粉末是金属铜,
,蓝色溶液是含有铜离子的溶液,结合上述分析,X粉末是金属铜,
故答案为:![]() ;
;![]() ;
;
(2)过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(3)X粉末是金属铜,黑色固体是氧化铜,所以蓝色溶液是硫酸铜,固体C是碳酸钠,和氢氧化钙反应生成碳酸钙和氢氧化钠,氢氧化钠可以和硫酸铜反应生成氢氧化铜和硫酸钠,反应②的离子方程式是:Cu2++2OH-=Cu(OH)2↓,
故答案为:Cu2++2OH-=Cu(OH)2↓。
(4)固体C是碳酸钠,除去碳酸碳中的碳酸氢钠可以采用加热的方法,方程式为:![]() ,
,
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是
A. NaHCO3水解的离子方程式:HCO3-+ H2O![]() CO32-+H3O+
CO32-+H3O+
B. NH4Cl溶于D2O中:NH4++D2O![]() NH3·HDO+D+
NH3·HDO+D+
C. Na2S显碱性原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
D. 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-=A2-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式中,正确的是( )
A. 稀硫酸滴在铜片上:Cu+2H+===Cu2++H2↑
B. 稀硫酸与Ba(OH)2溶液混合:SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. 稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D. 氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研究了在Cu-ZnO-ZrO2催化剂上CO2加氢制甲醇过程中水的作用机理,其主反应历程如图所示(H2→*H+* H)。下列说法错误的是

A.向该反应体系中加入少量的水能增加甲醇的收率
B.带*标记的物质是该反应历程中的中间产物
C.二氧化碳加氢制甲醇的过程中原子利用率达100%
D.第③步的反应式为*H3CO+ H2O→CH3OH+*HO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于沉淀溶解平衡和溶度积常数,下列说法不正确的是( )
A. Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关
B. 将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4)
C. 已知25 ℃时Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe(OH)3+3H+![]() Fe3++3H2O的平衡常数K=4.0×104
Fe3++3H2O的平衡常数K=4.0×104
D. 已知25 ℃时Ksp[Mg(OH)2] =1.8×10-11,在MgCl2溶液中加入氨水调混合液的pH=11,产生沉淀,则此时溶液中的c(Mg2+)=1.8×10-5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下有①6.72L CH4,②3.01×1023个HCl分子,③13.6g硫化氢,④0.2mol氨气(NH3)。下列对这四种气体的关系从大到小描述不正确的是( )
A.体积②>③>①>④B.密度②>③>④>①
C.质量②>③>①>④D.氢原子数①>④>③>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( )

A. 反应①中试剂X是氢氧化钠溶液
B. 反应①过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应中包含一个氧化还原反应
D. 将试剂X和Y进行对换,最终可以达到相同的效果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应过程中的先后顺序,下列评价正确的是
A.向浓度都为0.1mol/L的FeCl3和CuCl2加入铁粉,溶质CuCl2首先与铁粉反应
B.向过量的Ba(OH)2溶液中滴加少量的KAl(SO4)2溶液,开始没有白色沉淀生成
C.向浓度都为0.1mol/L 的Na2CO3和NaOH的混合溶液通入CO2气体,NaOH首先反应
D.向浓度为0.1mol/L的FeCl3溶液中,加入质量相同、颗粒大小相同的铁和铜,铜单质首先参加反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下面各个小题的要求填空
(1)有下列各组物质,将符合下方描述的组合对应的字母填在横线上
A.O2和O3 B.12C和13C C.甲烷和庚烷D.CH3CH2CH2CH3和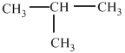 E.
E. 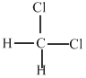 和
和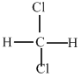
a.____________组两物质互为同位素。
b.____________组两物质互为同素异形体。
c.____________组两物质属于同系物。
d. ____________组两物质互为同分异构体。
(2)(1)①P4(s,白磷)+5O2(g)=P4O10(s) △H1=2983.2kJ/mol
②P(s,红磷)+5/4O2(g)=1/4P4O10(s),△H=738.5kJ/mol
根据上述信息,写出白磷转化为红磷的热化学方程式________.
(3)已知C2H4(g)和C2H5OH(l)的燃烧热分别是1141kJ/mol和1366.8kJ/mol,写出C2H4(g)和H2O(l)反应生成C2H5OH(l)的热化学方程式:_______。
(4)某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜。某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下气体6.72L(其中NO2和NO的体积比为2:1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比___________。
②反应后得到的溶液中H+的浓度为1.0mol/L,求原硝酸的物质的量浓度。(假设反应前后溶液的体积不变)_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com