
| A. | 先装好药品,再检查装置的气密性 | |
| B. | 先用双手握紧试管,再将导管插入水中检查装置气密性 | |
| C. | 结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管 | |
| D. | 稀释硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
分析 A.应先检查装置的气密性,再放药品;
B.先用手捂容器外壁,里面的空气受热膨胀会早逸出;
C.结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管,防止空气氧化Cu;
D.浓硫酸的密度比水的大,并且在溶解的过程中要放出大量的热.
解答 解:A.制备气体时,如果装置的气密性不好,就收集不到气体,故应先检查装置的气密性,再放药品,故A错误;
B.检查气密性时,要先把导管浸入水中再用手去捂容器外壁,若先用手捂容器外壁,里面的空气受热膨胀会早逸出,导致看不到导管口处冒气泡,顺序错误,故B错误;
C.结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管,防止空气氧化Cu生成CuO,故C正确;
D.浓硫酸的密度比水的大,溶于水时要放出大量的热,所以在稀释浓硫酸时要将浓硫酸注入水中并不断搅拌,使放出的热量及时散失,故D错误.
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及实验操作先后顺序判断,明确实验操作规范性及物质性质、实验原理是解本题关键,注意实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
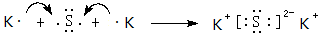 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

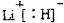 .
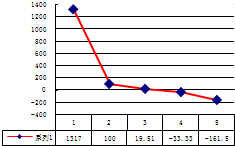
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,c(H+)/c(OH一)=1×10-12的溶液:K+、AlO2-、SiO32-、Na+ | |
| B. | 加入KSCN显红色的溶液:K+、NH4+、Cl-、I- | |
| C. | 加入石蕊显蓝色的溶液:Cu2+、Al3+、NO3-、SO42- | |
| D. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
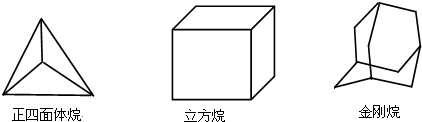
| A. | 2,4,8 | B. | 2,4,6 | C. | 1,3,6 | D. | 1,3,8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2 O2 | B. | Al(OH)3 AlCl3 | C. | FeCl3 Fe(OH)3 | D. | NaOH Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
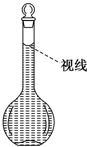 用18mol/L的浓硫酸配制80mL 1.0mol/L的稀硫酸,需用的实验仪器有:A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
用18mol/L的浓硫酸配制80mL 1.0mol/L的稀硫酸,需用的实验仪器有:A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应结束时溶液的pH=7 | |
| B. | 反应后溶液中存在的粒子只有Na+和Cl- | |
| C. | 该反应的实质是H+和OH-结合生成水 | |
| D. | 反应前后所有元素的化合价均无变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com