
|
| 2 |
| 2 |
| m |
| V |
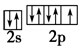 ���ʴ�Ϊ��F��
���ʴ�Ϊ��F�� ��
��| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 8 |
| 1 |
| 2 |
|
| 2 |
| 2 |
| m |
| V |
| ||
(2
|
| M | ||
4
|
| M | ||
4
|


 ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���ƶ�����غ�����������ʵķ���������һ��CH2����������ͬϵ�� |
B����ϵͳ���������л���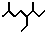 ������Ϊ2��6-����-4-�һ����� ������Ϊ2��6-����-4-�һ����� |
| C������������ڹ������ȡ����Ӧ����Ϊ�������£��������ʧȥһ����ԭ�Ӻͼ���������Cl2��ײ����CH3Cl�������ɻ���Cl?�� |
D�����⾫ѧ���������ޣ��ṹ��ͼ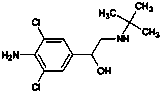 �����Է���ȡ�����ӳɡ�ˮ�⡢��������ȥ��Ӧ �����Է���ȡ�����ӳɡ�ˮ�⡢��������ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
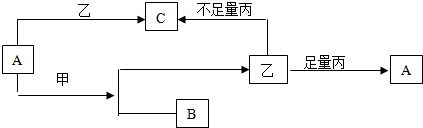
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
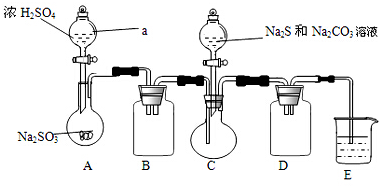
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
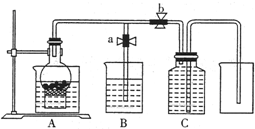 ijͬѧ�����ͼ��ʾװ���������ô�������ijŨ��ϡ���ᷴӦ��ȡNO���壮
ijͬѧ�����ͼ��ʾװ���������ô�������ijŨ��ϡ���ᷴӦ��ȡNO���壮
|
������Һ�е������Ӽ������ʵ��� | ||||
��
|
|||||
=
|
a mol Fe3+ | ||||
����
|
|||||
=
|
a mol Fe2+ | ||||
��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�106g̼���ƹ��������е������ܵ����ʵ���С��3mol |
| B����ͬѹ��ͬ�µ�����£�������ͬ�������ͳ���������ԭ��������ͬ |
| C�������ʵ���Ũ�ȷֱ�Ϊ1mol/L��2mol/L�������������ϣ�����������ԼӺͣ������Ϻ�������Һ��Ũ��Ϊ1.5mol/L |
| D������£�22.4L CH3Cl������ԼΪ6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
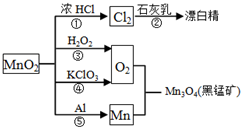
| A����Ӧ�٢ڢۢܢݾ�����������Ӧ�����ӷ�Ӧ |
| B����Ӧ��˵�������������Ļ�ԭ��ǿ���� |
| C����ͬ���������ɵ�����O2����Ӧ�ۺ͢�ת�Ƶĵ�����֮��Ϊ1��1 |
| D����Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�����ȷ�������Fe2O3+2Al
| ||||
B����ҵ����NH3�Ʊ�NO��4NH3+5O2
| ||||
| C����������Ӱ��ĺ���������CaCO3��ĩ��CO32-+2H+�TH2O+CO2�� | ||||
| D�������������ں����������Ϊ��������Դ��2Na2O2+2CO2�T2Na2CO3+O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
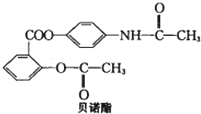
| A������ʽΪC17H14O5N |
| B������������ˮ��Һ��ˮ����Եõ�3���л������� |
| C��1mol��ŵ����H2�����ӳɷ�Ӧ�������8mol H2 |
| D����ŵ�����������������ڵ������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com