
| A. | Ba(OH)2•8H2O与NH4Cl反应 | |
| B. | 铝与稀盐酸 | |
| C. | 灼热的炭与水蒸气生成一氧化碳和氢气的反应 | |
| D. | 煤与O2的燃烧反应 |
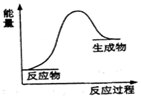
分析 由图可知反应物总能量小于生成物总能量,为吸热反应,且属于氧化还原反应,则应存在元素化合价的变化,以此解答该题.
解答 解:A.Ba(OH)2•8H2O与NH4Cl反应,生成氯化钡、氨气和水,元素化合价没有变化,不是氧化还原反应,故A错误;
B.铝与盐酸的反应为放热反应,故B错误;
C.灼热的炭与水蒸气生成一氧化碳和氢气的反应,C、H元素化合价变化,属于氧化还原反应,且为吸热反应,故C正确;
D.煤与O2的燃烧反应属于放热反应,故D错误.
故选C.
点评 本题综合考查氧化还原反应以及反应热与焓变,为高频考点,侧重考查学生的分析能力,注意把握常见吸热反应、放热反应以及氧化还原反应的特点,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
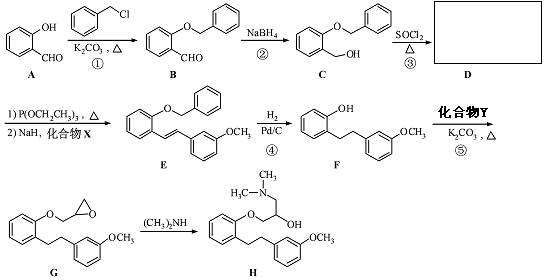

 .
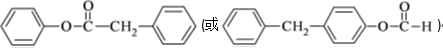
.
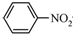 $→_{Pd/C}^{H_{2}}$
$→_{Pd/C}^{H_{2}}$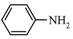 .化合物
.化合物  是合成抗癌药物美法
是合成抗癌药物美法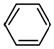 和
和 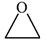 为原料制备该化合物的合成路线流程图(无机试剂任
为原料制备该化合物的合成路线流程图(无机试剂任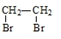
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 除①④⑥以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(ClO)2溶液中通入CO2至过量 | |
| B. | 向Na2SiO3溶液中滴加盐酸溶液至过量 | |
| C. | 向氢氧化铁胶体中滴加稀硫酸至过量 | |
| D. | 向Na[Al(OH)4]溶液中滴加盐酸至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO | B. | MnO2 | C. | Fe2O3 | D. | Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com