
| A. | a=2,b=1 | B. | a=3,b=2 | C. | a=2,b=2 | D. | a=3,b=3 |
分析 1mol X气体跟a mol Y气体在体积可变的密闭容器中反应,反应达到平衡后,测得X的转化率为50%,则参加反应的X为0.5mol,则:
X(g)+a Y(g)?b Z(g)
起始量(mol):1 a 0
变化量(mol):0.5 0.5a 0.5b
平衡量(mol):0.5 0.5a 0.5b
同温同压下,气体总质量不变,反应前后混合气体的密度之比和气体体积成反比,即和气体物质的量成反比,反应前混合气体的密度是反应后混合气体密度的$\frac{3}{4}$,则反应前气体物质的量是反应后气体物质的量$\frac{4}{3}$,则(1+a):(0.5+0.5a+0.5b)=4:3,以此解答该题.
解答 解:1mol X气体跟a mol Y气体在体积可变的密闭容器中反应,反应达到平衡后,测得X的转化率为50%,则参加反应的X为0.5mol,则:
X(g)+a Y(g)?b Z(g)
起始量(mol):1 a 0
变化量(mol):0.5 0.5a 0.5b
平衡量(mol):0.5 0.5a 0.5b
同温同压下,气体总质量不变,反应前后混合气体的密度之比和气体体积成反比,即和气体物质的量成反比,反应前混合气体的密度是反应后混合气体密度的$\frac{3}{4}$,则反应前气体物质的量是反应后气体物质的量$\frac{4}{3}$,则(1+a):(0.5+0.5a+0.5b)=4:3,
计算得到:2b=a+1;
依据选项中的取值分析判断,a=3,b=2符合计算关系.
故选B.
点评 本题考查了化学平衡的计算,为高频考点,侧重考查学生的分析能力和计算能力,明确同温同压下混合气体密度之比和气体物质的量成反比是计算关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | H2O | B. | HCl溶液 | C. | H2SO4溶液 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用锌与稀硫酸反应制备氢气时,加入少量硫酸铜 | |
| B. | Al与稀硫酸反应制取H2时,改用质量分数为98.3%的浓硫酸 | |
| C. | Fe与稀硫酸反应时,把铁粉改为铁片 | |
| D. | Na与水反应时增大水的用量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、C2H4 | B. | C2H6、C3H6 | C. | CH4、C2H6 | D. | C2H6、C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2S是唯一的还原产物 | |
| B. | 反应中的氧化剂只有CuSO4 | |
| C. | 被氧化与被还原硫元素的质量比为7:3 | |
| D. | 若以该反应为原理设计原电池,电池的正极为石墨棒,负极是吸附有FeS2粉末的多孔石墨电极,电解质溶液为CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
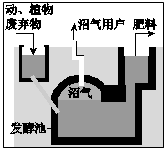 阅读下文,回答问题.
阅读下文,回答问题. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 (1)a图中的图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是3.2mL.
(1)a图中的图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是3.2mL.| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ③④⑤ | D. | ①④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com