
下列物质中,既含离子键又含共价键的是
A.HCl B.NaOH C.NaCl D.O2
科目:高中化学 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
对发现元素周期律贡献最大的化学家是 ( )
A.牛顿 B.道尔顿 C.阿伏加德罗 D.门捷列夫
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
假酒中严重超标的有毒成分是:
A.CH3CH2OH B.CH3OH C.CH3COOCH2CH3 D.CH3COOH
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
下列化学变化中,能够一步实现的是
A.Na→Na2O2 B.Al2O3→Al(OH)3 C.N2→HNO3 D.S→SO3
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
下列物质中,S元素的化合价为+6的是
A.S B.H2SO4 C.SO2 D.H2S
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省广州市越秀区高二下学期期末水平调研化学试卷(解析版) 题型:填空题
某芳香烃A是有机合成中重要的原料,通过质谱法测得其相对分子质量为118,其苯环上只有一个取代基。以下是以A为原料合成化合物F和高分子化合物I的路线图,其中化合物F中含有三个六元环。试回答下列问题:
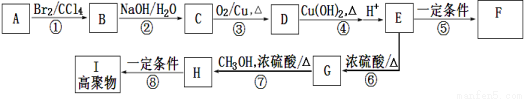
(1)E中官能团的名称为 ;
(2)I的结构简式为 ;
(3)写出反应③的化学方程式 ;
(4)写出反应⑤的化学方程式 ;
(5)写出所有符合下列要求的D的同分异构体的结构简式 ;
a.苯环上只有一个取代基; b.能与新制氢氧化铜悬浊液反应;
c.分子中—COO—含有结构。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省广州市越秀区高二下学期期末水平调研化学试卷(解析版) 题型:选择题
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
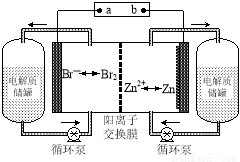
A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高三5月第三次模拟理综化学试卷(解析版) 题型:填空题
(16分)海水资源的利用具有广阔前景。海水中主要离子的含量如下:
成分 | 含量/(mg?L-1) | 成分 | 含量/(mg?L-1) |
Cl- | 18980 | Ca2+ | 400 |
Na+ | 10560 | HCO3- | 142 |
SO42 | 2560 | Br- | 64 |
Mg2+ | 1272 |
|
|
电渗析法淡化海水示意图如图所示,其中阴(阳)
离子交换膜仅允许阴(阳)离子通过。

①阳极主要电极反应式是 。
②在阴极附近产生少量白色沉淀,其成分有 和CaCO3,
生成CaCO3的离子方程式是 。
③淡水的出口为 (填“a”、“b”或“c”)。
(2)利用海水可以提取溴和镁,提取过程如下: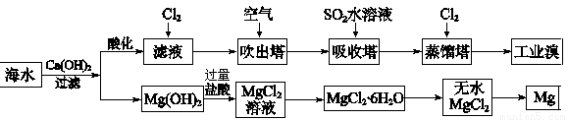
①提取溴的过程中,经过2次Br-→Br2转化的目的是 ,吸收塔中发生反应的离子方程式是 。解释通空气的目的是 。
②从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是 、过滤、洗涤、干燥。
③依据上述流程,若将10 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
L(忽略Cl2溶解,溴的相对原子质量:80)。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省高二下学期期中化学试卷(解析版) 题型:选择题
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属于离子型碳化物,请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是?
A.ZnC2水解生成乙烷 B.Al4C3水解生成甲烷?
C.Mg2C3水解生成丙烯 D.Li2C2水解生成乙炔?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com