
下列溶液中,溶质的物质的量浓度为1 mol·L-1 的是( )
A.将40 g NaOH溶于1 L 水所得的溶液
B.将0.5 mol·L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液
C.将23 g Na 溶于1 L水并配成溶液
D.含K+为2 mol·L-1的K2SO4溶液
科目:高中化学 来源: 题型:
将4.6 g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还原产物为4480mL NO2气和336 mL N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为 ( )
A.9.02 g B.8.51 g C.8.26 g D.7.04 g
查看答案和解析>>
科目:高中化学 来源: 题型:
镁、铝能够在空气中稳定存在的原因是( )。
A.性质不活泼,不与空气中的成分反应
B.镁、铝与氧气的反应速率极慢
C.经过了特殊工艺处理
D.与氧气反应形成了氧化物保护膜
查看答案和解析>>
科目:高中化学 来源: 题型:
想一想: HCl(气态)、CH3COOH(液态)、Ba(OH)2(固态)、CuSO4(固态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类 ( )
A.C2H5OH溶液 B.Na2CO3·10H2O C.水煤气 D.豆浆
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式的是 ( )
A.氢氧化钡溶液与硫酸的反应 OH-+H+ = H2O
B.金属镁与稀盐酸反应 Mg + 2H++2 Cl-= MgCl2 + H2
C.金属钠投入到冷水中 Na+ H2O= Na+ + OH-+ H2↑
D.氯气通入氢氧化钠溶液中 Cl2+2OH-=Cl-+ ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要0.1 mol/L NaOH溶液450 mL和0.6 mol/L硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
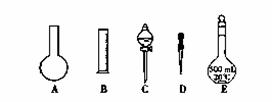 ①如图所示的仪器中,配制溶液肯定不需要的是_________ (填序号),配制上述溶液还需用到的玻璃仪器有 (填仪器名称)。
①如图所示的仪器中,配制溶液肯定不需要的是_________ (填序号),配制上述溶液还需用到的玻璃仪器有 (填仪器名称)。
②配制0.1 mol/L NaOH溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次)
。
A.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
B.将容量瓶盖紧,振荡,摇匀
C.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
D.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约100mL),用玻璃棒慢慢搅动,使其充分溶解。
E.将溶解、冷却后的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
F.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
③配制0.1 mol/L NaOH溶液时,在实验中其他操作均正确,若定容时俯视容量瓶刻度线,则所配溶液浓度 0.1 mol/L(填“大于”、“等于”或“小于”)。
④配制0. 6 mol/L硫酸溶液500 mL时,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。
⑤配制0.6 mol/L硫酸溶液时,在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所配溶液浓度 0.6 mol/L(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应前后肯定没有变化的是
①原子数目 ②分子数目 ③元素种类
④物质的总质量 ⑤物质的种类
A. ①④ B. ①③⑤ C. ①③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
阅读、分析下列两个材料:
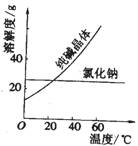 材料一、
材料一、
材料二、
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题(填写序号):
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
(1) 将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用__________。
(2)将乙二醇和丙三醇相互分离的最佳方法是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
查阅资料发现,金属钠不仅能够跟氧气和水反应,还能与酒精在常温下反应,要研究金属钠和酒精反应的性质以及它与金属钠跟水反应的异同点,下列研究方法中用不到的是( )
A.分类法 B.观察法
C.实验法 D.比较法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com