
【题目】科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为对人体无害的![]() 价砷类化合物在维生素C的作用下,能够转化为有毒的
价砷类化合物在维生素C的作用下,能够转化为有毒的![]() 价的含砷化合物。通过以上信息填空:
价的含砷化合物。通过以上信息填空:
①维生素C具有______(填“氧化性”或“还原性”)。
②3mol +5价砷完全转化为![]() 价砷,共转移______个电子。
价砷,共转移______个电子。
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.常温常压下,1 NA 个CO2分子占有的体积为22.4L
B.常温常压下,14gN2含有原子数为0.5NA
C.常温常压下,14gCO的质子数为7NA
D.74.5 g KCl固体中含有KCl分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将如图所示实验装置的K闭合,下列判断不正确的是( )
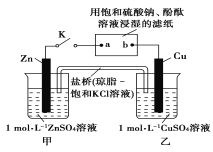
A.Cu电极上发生还原反应
B.片刻后甲池中c(SO42-)不变
C.电子沿Zn→a→b→Cu路径流动
D.片刻后可观察到滤纸a点变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物其结构如图所示,下列说法中正确的是()
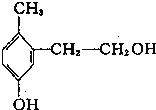
A.它是苯酚的同系物
B.1mol有机物能与2molNaOH反应
C.1mol该有机物能与金属钠反应产生![]()
D.1mol该有机物能与溴水反应消耗2mol![]() 发生取代反应
发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
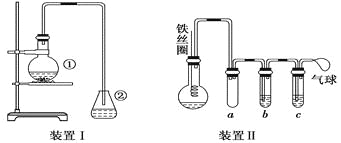
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
(1)装置I中①的化学方程式为__________________________________________.
②中离子方程式为__________________________________________________.
(2)①中长导管的作用是________________________________________________.
(3)烧瓶中生成的红褐色油状液滴的成分是__________________________,要想得到纯净的产物,可用__________________________试剂洗涤.洗涤后分离粗产品应使用的仪器是____________________.
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验.可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳.
a的作用是__________________________________________________________.
b中的试剂是__________________________________________________________.
比较两套装置,装置Ⅱ的主要优点是______________________________________
________________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是
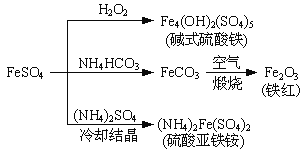
A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体 ,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现红色。
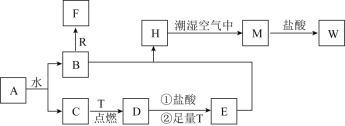
(1)物质D的化学式为___________,H的名称___________。
(2)![]() 在潮湿空气中变成M的实验现象是______________,化学方程式为___________。
在潮湿空气中变成M的实验现象是______________,化学方程式为___________。
(3)![]() 与W溶液也能发生反应,其反应的类型为______(填序号)。
与W溶液也能发生反应,其反应的类型为______(填序号)。
![]() 化合反应
化合反应 ![]() 置换反应
置换反应 ![]() 复分解反应
复分解反应 ![]() 氧化还原反应
氧化还原反应
(4)![]() 和R在溶液中反应生成F的离子方程式为____________________。
和R在溶液中反应生成F的离子方程式为____________________。
(5)将![]() 投入到E溶液中,可以观察到的现象是:___________________。
投入到E溶液中,可以观察到的现象是:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)的流程如下:

回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是________(填序号)。
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是________________(填化学式)。
(3)“沉淀反应”时反应温度不宜过高,其原因为________(用化学方程式表示)。
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加________溶液。
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为________。
(6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为________。(提示:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在pH=5的CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入水时,平衡向右移动,CH3COOH电离常数增大
B.加入少量CH3COONa固体,平衡向右移动
C.加入少量NaOH固体,平衡向右移动,c(H+)减小
D.加入少量pH=5的硫酸,溶液中c(H+)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com