
| A. |  干燥Cl2 | |
| B. |  配制100 mL 0.1 mol•L-1 硫酸溶液 | |
| C. |  分离沸点相差较大的互溶液体混合物 | |
| D. |  分离互不相溶的两种液体 |
分析 A.根据使用浓硫酸干燥Cl2时,进气导管应伸入浓硫酸的液面以下分析;
B.不能在容量瓶中稀释浓硫酸;
C.从温度计的使用目的角度分析解答;
D.根据分液实验的规范操作分析.
解答 解:A.图示的干燥装置中,进气导管连接错误,无法对Cl2进行干燥,图中操作错误应长管进短管出,故A错误;
B.容量瓶上有刻度,热胀冷缩影响其配制溶液的精确度,所以不能在容量瓶中稀释浓硫酸,应在烧杯中稀释后转移到容量瓶中,故B错误;
C.分离沸点相差较大的互溶液体混合物蒸馏时,温度计水银球应在蒸馏烧瓶支管口正中央,测不同液体的沸点,故C错误;
D.分离互不相溶的两种液体,可用分液的方法分离、提纯;分液时,密度大的液体在下方,为防止产生杂质,下层液体从下口流出,上层液体从上口倒出,故D正确;
故选D.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应将混合物中的水分蒸干后,才能停止加热 | |
| B. | 用Ba(NO3)2溶液鉴别Cl-、SO42和CO32- | |
| C. | 用氨水鉴别Al3+、Mg2+和Ag+ | |
| D. | 可以用溶解过滤的方法从加热氯酸钾和二氧化锰的混合物中获得二氧化锰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 经常使用一次性筷子、纸杯、塑料袋等做法能保护环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
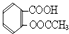 ).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:

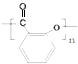 .
.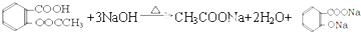 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
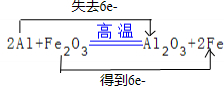
 ,它是由Na+与O22-(填写离子符号)构成的.
,它是由Na+与O22-(填写离子符号)构成的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA | |
| B. | 1molAl3+含有核外电子数为3NA | |
| C. | 常温常压下,1mol氧气所含的原子数为NA | |
| D. | 1molNaCl晶体中含有NA个Na+和NA个Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 残留固体中一定不含有铁 | B. | 滤液中可能含有Fe3+ | ||
| C. | 原混合物中n(Fe)=n(Fe2O3)+n(CuO) | D. | 原混合物中铁为3.36 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
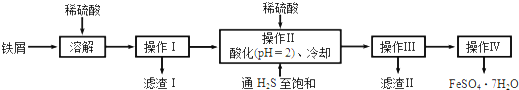
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
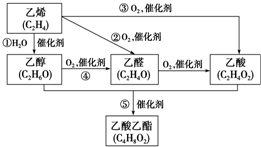 如图是由乙烯合成乙酸乙酯的几种可能的合成路线:
如图是由乙烯合成乙酸乙酯的几种可能的合成路线: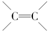 ,乙醇中含氧官能团的名称是羟基;
,乙醇中含氧官能团的名称是羟基;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com