
| A、1:2 | B、1:3 |
| C、2:3 | D、2:1 |
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
| A、室温下,0.1mol?L-1的CH3COONa溶液的pH=8 |
| B、醋酸与CaCO3反应有气体生成 |
| C、室温下,0.1mol?L-1的CH3COOH溶液的pH=3 |
| D、醋酸中加水后,溶液的pH升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中“氮的固定” |
| B、用铂丝蘸取NaCl溶液进行焰色反应 |
| C、食物腐败变质 |
| D、铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径呈周期性变化 |
| B、元素化合价呈周期性变化 |
| C、电子层数逐渐增加 |
| D、元素原子的核外电子排布呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA | ||
| B、1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | ||
| C、常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子 | ||
D、将CO2通过Na2O2使其增重a g,反应中转移的电子数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、工业合成氨:N2+3H2
| |||
B、工业合成盐酸:H2+Cl2
| |||
C、工业获取氯化钠:2Na+Cl2
| |||
D、工业制取氯气:2NaCl+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
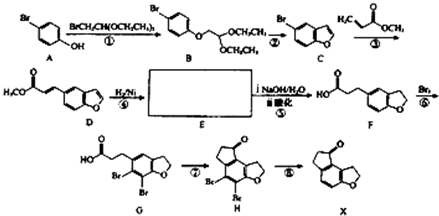
查看答案和解析>>
科目:高中化学 来源: 题型:
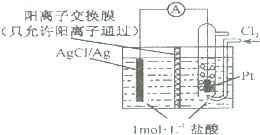
| A、正极反应为Cl2-2e-=2Cl- |
| B、放电时H+从右侧经阳离子交换膜移向左侧 |
| C、电路中转移0.01 mole-时,交换膜左侧溶液中减少0.01 mol离子 |
| D、若用NaCl溶液代替盐酸,电池的总反应不会改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com