
 ÓŠa”¢bĮ½øö¼«Ņ×µ¼ČȵÄĆܱÕČŻĘ÷£¬a±£³ÖČŻ»ż²»±ä£¬bÖŠµÄ»īČūæÉÉĻĻĀŅĘ¶Æ£¬ŅŌ±£³ÖÄŚĶāŃ¹ĒæĻąµČ£®ŌŚĻąĶ¬Ģõ¼žĻĀ½«3molA”¢1molB·Ö±šĶ¬Ź±»ģŗĻÓŚa”¢bĮ½ČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ
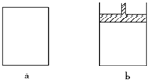
ÓŠa”¢bĮ½øö¼«Ņ×µ¼ČȵÄĆܱÕČŻĘ÷£¬a±£³ÖČŻ»ż²»±ä£¬bÖŠµÄ»īČūæÉÉĻĻĀŅĘ¶Æ£¬ŅŌ±£³ÖÄŚĶāŃ¹ĒæĻąµČ£®ŌŚĻąĶ¬Ģõ¼žĻĀ½«3molA”¢1molB·Ö±šĶ¬Ź±»ģŗĻÓŚa”¢bĮ½ČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ·ÖĪö £Ø1£©a±£³ÖČŻ»ż²»±ä£¬b±£³ÖÄŚĶāŃ¹ĒæĻąµČ£¬·“Ó¦3A£Øg£©+B£Øg£©?2C£Øg£©+D£Øg£©ŹĒĘųĢåĪļÖŹµÄĮæ¼õÉŁµÄ·“Ó¦£¬Ę½ŗāŹ±aÖŠŃ¹Ēæ±ČbÖŠŠ”£¬¹ŹbĻąµ±ÓŚŌŚaĘ½ŗāµÄ»ł“”ÉĻ¼ÓŃ¹£¬Ę½ŗāÓŅŅĘ£¬Ę½ŗāŅĘ¶Æ²»ÄÜĻū³żAµÄÅضČŌö“󣬵½“ļŠĀĘ½ŗāŹ±µÄÅضČøßÓŚŌĘ½ŗā£»
£Ø2£©øıäĘšŹ¼Ķ¶ĮĻ±Č£¬ŅŖĻė“ļµ½Ę½ŗāŗóaÖŠCµÄÅضČČŌĪŖN mol•L-1£¬ŗćĪĀŗćČŻĻĀ£¬ÓėŌĘ½ŗāŹĒĶźČ«µČŠ§Ę½ŗā£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½·½³ĢŹ½×ó±ß£¬Āś×ćÓėŌĘ½ŗāÖŠĻąĶ¬ĪļÖŹµÄĘšŹ¼Ķ¶ĮĻĮæĻąµČ£»
bÖŠCµÄÅضČĪŖn mol•L-1£¬ÓėŌĘ½ŗāĪŖµČŠ§Ę½ŗā£¬µČĪĀµČŃ¹µÄĢõ¼žĻĀ£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½·½³ĢŹ½×ó±ß£¬Āś×ćÓėŌĘ½ŗāÖŠĪļÖŹµÄĶ¶ĮĻĮæ±Č£»
£Ø3£©Čō½«2molCŗĶ2molD³äČėaÖŠ£¬µČŠ§ĪŖæŖŹ¼Ķ¶Čė3molA£Øg£©”¢1molB£Øg£©”¢1molD£Øg£©£¬ÓėŌĘ½ŗāĻą±ČĘ½ŗāÄęĻņŅĘ¶Æ£»
£Ø4£©½«4 mol CŗĶ2 mol D³äČėaÖŠĻąµ±ÓŚæŖŹ¼³äČė6 mol A”¢2 mol B£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬·“Ó¦Īļ×Ŗ»ÆĀŹŌö“󣬲Ī¼Ó·“Ó¦µÄAµÄĪļÖŹµÄĮæ“óÓŚŌĘ½ŗāµÄ2±¶£¬Ę½ŗāŅĘ¶Æ²»ÄÜĻū³żAµÄÅضČŌö“󣬵½“ļŠĀĘ½ŗāŹ±µÄÅضČøßÓŚŌĘ½ŗā£®
½ā“š ½ā£ŗ£Ø1£©a±£³ÖČŻ»ż²»±ä£¬b±£³ÖÄŚĶāŃ¹ĒæĻąµČ£¬·“Ó¦3A£Øg£©+B£Øg£©?2C£Øg£©+D£Øg£©ŹĒĘųĢåĪļÖŹµÄĮæ¼õÉŁµÄ·“Ó¦£¬Ę½ŗāŹ±aÖŠŃ¹Ēæ±ČbÖŠŠ”£¬¹ŹbĻąµ±ÓŚŌŚaĘ½ŗāµÄ»ł“”ÉĻ¼ÓŃ¹£¬Ę½ŗāÓŅŅĘ£¬Ę½ŗāŅĘ¶Æ²»ÄÜĻū³żAµÄÅضČŌö“󣬵½“ļŠĀĘ½ŗāŹ±µÄÅضČøßÓŚŌĘ½ŗā£¬¹ŹbÖŠĘ½ŗāŹ±AµÄÅØ¶Č“óÓŚaÖŠAµÄĘ½ŗāÅØ¶Č£¬¼“M£¼m£¬Ę½ŗāÓŅŅĘ£¬bÖŠCµÄĘ½ŗāÅضČøßÓŚaÖŠCµÄĘ½ŗāÅØ¶Č£¬¼“N£¼n£¬
¹Ź“š°øĪŖ£ŗ£¼£»£¼£»
£Ø2£©øıäĘšŹ¼Ķ¶ĮĻ±Č£¬ŅŖĻė“ļµ½Ę½ŗāŗóaÖŠCµÄÅضČČŌĪŖN mol•L-1£¬ŗćĪĀŗćČŻĻĀ£¬ÓėŌĘ½ŗāŹĒĶźČ«µČŠ§Ę½ŗā£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½·½³ĢŹ½×ó±ß£¬Āś×ćÓėŌĘ½ŗāÖŠĻąĶ¬ĪļÖŹµÄĘšŹ¼Ķ¶ĮĻĮæĻąµČ£¬Ń”ĻīÖŠDE·ūŗĻ£»
bÖŠCµÄÅضČĪŖn mol•L-1£¬ÓėŌĘ½ŗāĪŖµČŠ§Ę½ŗā£¬µČĪĀµČŃ¹µÄĢõ¼žĻĀ£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½·½³ĢŹ½×ó±ß£¬Āś×ćÓėŌĘ½ŗāÖŠĪļÖŹµÄĶ¶ĮĻĮæ±Č£¬Ń”ĻīÖŠADE·ūŗĻ£¬
¹Ź“š°øĪŖ£ŗDE£»ADE£»
£Ø3£©Čō½«2molCŗĶ2molD³äČėaÖŠ£¬µČŠ§ĪŖæŖŹ¼Ķ¶Čė3molA£Øg£©”¢1molB£Øg£©”¢1molD£Øg£©£¬ÓėŌĘ½ŗāĻą±ČĘ½ŗāÄęĻņŅĘ¶Æ£¬¹ŹĘ½ŗāŹ±AµÄÅضČŌö“ó£¬CµÄÅØ¶Č¼õŠ”£¬¼“W£¾M”¢Y£¼N£¬
¹Ź“š°øĪŖ£ŗ£¾£»£¼£»
£Ø4£©½«4mol CŗĶ2 mol D³äČėaÖŠĻąµ±ÓŚæŖŹ¼³äČė6 mol A+2 mol B£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņÓŅŅĘ¶Æ£¬·“Ó¦Īļ×Ŗ»ÆĀŹŌö“󣬲Ī¼Ó·“Ó¦µÄAµÄĪļÖŹµÄĮæ“óÓŚŌĘ½ŗāµÄ2±¶£¬Ę½ŗāŹ±AµÄÅØ¶ČŠ”ÓŚŌĘ½ŗāµÄ2±¶£¬Ę½ŗāŅĘ¶Æ²»ÄÜĻū³żAµÄÅضČŌö“󣬵½“ļŠĀĘ½ŗāŹ±µÄÅضČøßÓŚŌĘ½ŗā£¬¹ŹM£¼R£¼2M£¬
¹Ź“š°øĪŖ£ŗC£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāŅʶÆÓė¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬ÄѶČÖŠµČ£¬×¢ŅāĄūÓƵȊ§Ė¼ĻėÉč¼ĘĘ½ŗā½ØĮ¢µÄĶ¾¾¶£¬Ąķ½āµČŠ§Ę½ŗā¹ęĀÉ£ŗ1”¢ŗćĪĀŗćČŻ£¬·“Ó¦Ē°ŗóĘųĢåĢå»ż²»µČ£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½Ņ»±ß£¬¶ŌÓ¦ĪļÖŹĀś×ćµČĮ棻·“Ó¦Ē°ŗóĘųĢåĢå»żĻąµČ£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½Ņ»±ß£¬¶ŌÓ¦ĪļÖŹĀś×ćµČ±Č£¬2£ŗŗćĪĀŗćŃ¹£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½Ņ»±ß£¬¶ŌÓ¦ĪļÖŹĀś×ćµČ±Č£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ¹ć¶«Ź”ɽŅ»øßČżÉĻµŚ¶ž“ĪĶ³²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
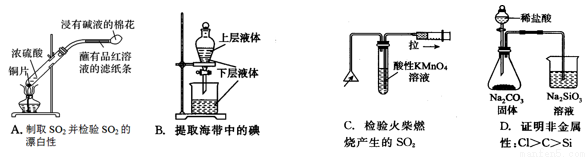
ĻĀĮŠŹµŃé×°ÖĆÕżČ·ĒŅÄÜĶź³ÉŹµŃéÄæµÄµÄŹĒ£Ø £©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
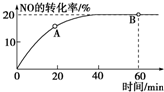 £Ø1£©Ä³ĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ1LµÄČŻĘ÷ÖŠ³äČė3mol NOŗĶ1mol CO£¬·¢Éś2NO£Øg£©+2CO£Øg£©???N2£Øg£©+2CO2£Øg£©·“Ó¦£¬NOµÄ×Ŗ»ÆĀŹĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾£®
£Ø1£©Ä³ĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ1LµÄČŻĘ÷ÖŠ³äČė3mol NOŗĶ1mol CO£¬·¢Éś2NO£Øg£©+2CO£Øg£©???N2£Øg£©+2CO2£Øg£©·“Ó¦£¬NOµÄ×Ŗ»ÆĀŹĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
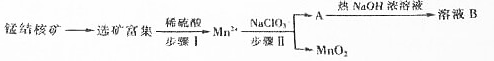
| »ÆŗĻĪļ | Zn£ØOH£©2 | Fe£ØOH£©2 | Fe£ØOH£©3 |
| Ksp½üĖĘÖµ | 10-17 | 10-17 | 10-39 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
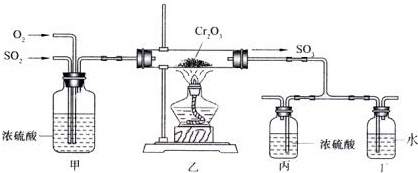
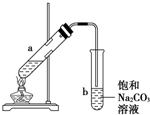 ČēĶ¼ĪŖŹµŃéŹŅÖĘȔɣĮæŅŅĖįŅŅõ„µÄ×°ÖĆĶ¼£¬ĻĀĮŠ¹ŲÓŚøĆŹµŃéµÄŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ĪŖŹµŃéŹŅÖĘȔɣĮæŅŅĖįŅŅõ„µÄ×°ÖĆĶ¼£¬ĻĀĮŠ¹ŲÓŚøĆŹµŃéµÄŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ĻņaŹŌ¹ÜÖŠĻČ¼ÓČėŅŅ“¼£¬Č»ŗó±ßŅ”¶ÆŹŌ¹Ü±ßĀżĀż¼ÓČėÅØĮņĖį£¬ŌŁ¼Ó±ł“×Ėį | |
| B£® | ŹŌ¹ÜbÖŠµ¼Ęų¹ÜĻĀ¶Ė¹ÜæŚ²»ÄܽžČėŅŗĆęµÄŌŅņŹĒ·ĄÖ¹ŹµŃé¹ż³ĢÖŠ·¢Éśµ¹ĪüĻÖĻó | |
| C£® | ŹµŃ鏱¼ÓČČŹŌ¹ÜaµÄÄæµÄŹĒ¼°Ź±½«ŅŅĖįŅŅõ„Õō³ö²¢¼Óæģ·“Ó¦ĖŁĀŹ | |
| D£® | æɽ«±„ŗĶĢ¼ĖįÄĘČÜŅŗ»»³ÉĒāŃõ»ÆÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
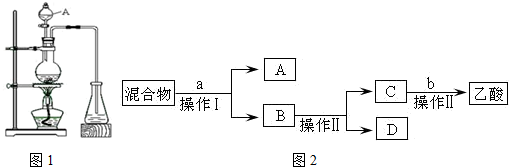
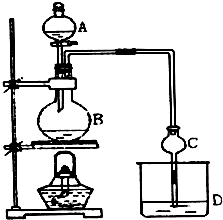 ijæĪĶāŠ”×éÉč¼ĘµÄŹµŃéŹŅÖĘČ”ŅŅĖįŅŅõ„µÄ×°ÖĆČēĶ¼ĖłŹ¾£¬AÖŠ·ÅÓŠÅØĮņĖį£¬BÖŠ·ÅÓŠŅŅ“¼”¢ĪŽĖ®“×ĖįÄĘ£¬DÖŠ·ÅÓŠ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£®
ijæĪĶāŠ”×éÉč¼ĘµÄŹµŃéŹŅÖĘČ”ŅŅĖįŅŅõ„µÄ×°ÖĆČēĶ¼ĖłŹ¾£¬AÖŠ·ÅÓŠÅØĮņĖį£¬BÖŠ·ÅÓŠŅŅ“¼”¢ĪŽĖ®“×ĖįÄĘ£¬DÖŠ·ÅÓŠ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£®| ŹŌ¼Į | ŅŅĆŃ | ŅŅ“¼ | ŅŅĖį | ŅŅĖįŅŅõ„ |
| ·Šµć£Ø”ę£© | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OC2H5+H2O£®
CH3CO18OC2H5+H2O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com