

| �������� | Fe��OH��3 | Fe��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 |
| ������ȫ��pH | 3.7 | 9.7 |
���� ��SrCO3Ϊԭ���Ʊ���ˮ�Ȼ��ȣ�SrCl2•6H2O���������̿�֪��SrCO3�����ᷢ����Ӧ��SrCO3+2HCl=SrCl2+CO2��+H2O����Ӧ����Һ�г�����Sr2+��Cl-�⣬����������Fe2+��Ba2+���ʣ�����������⣬��Fe2+����ΪFe3+��Ȼ��������������ᱵ������ͬʱ������ҺpH��ʹFe3+ת�������������������Թ��˺�����Ϊ���ᱵ��������������Һ�к�SrCl2�������������ȴ�ᾧ�õ�SrCl2•6H2O��
��1�������������Ũ�ȣ����ȵȿ�������Ӧ���ʣ�̼���������ᷴӦ�����Ȼ��ȡ�������̼��ˮ��
��2������Fe3+��ʼ����pH�������ȫpH������Һ��pH��Χ��������ҺpHʹFe3+ת�����������������Ҳ������������ʣ�
��3��SrCO3�����ᷴӦ����Һ�г�����Sr2+��Cl-�⣬����������Fe2+��Ba2+���ʣ�������ϡ���ᣬ�����ᱵ���ɣ�����������⣬��Fe2+����ΪFe3+���ٵ�����ҺpH��ˮ���������������������
��4��������ˮ�Ȼ��Ⱦ��忪ʼʧȥ�ᾧˮ���¶�ѡ���ȷ紵��ʱ���˵��¶ȣ�
��5�������ܽ�ƽ���Ҳ������������ʷ������
��� �⣺��SrCO3Ϊԭ���Ʊ���ˮ�Ȼ��ȣ�SrCl2•6H2O���������̿�֪��SrCO3�����ᷢ����Ӧ��SrCO3+2HCl=SrCl2+CO2��+H2O����Ӧ����Һ�г�����Sr2+��Cl-�⣬����������Fe2+��Ba2+���ʣ�����������⣬��Fe2+����ΪFe3+���������������ᱵ�������ٵ�����ҺpH��ʹFe3+ת�������������������Թ��˺�����Ϊ���ᱵ��������������Һ�к�SrCl2�������������ȴ�ᾧ�õ�SrCl2•6H2O��
��1�����������Ũ�ȣ����ȣ����߽��裬����Ӵ��������������Ӧ���ʣ�
̼���������ᷴӦ�����Ȼ��ȡ�������̼��ˮ����Ӧ�����ӷ���ʽΪSrCO3+2H+=Sr2++CO2��+H2O��
�ʴ�Ϊ�����ȡ��ʵ���������Ũ�ȵȣ�SrCO3+2H+=Sr2++CO2��+H2O��
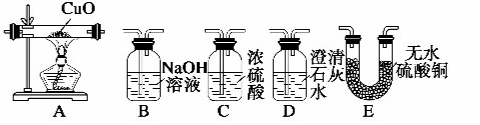
��2���ɱ������ݿ�֪��Fe3+��pH=1.5ʱ��ʼ��������pH=3.7ʱ������ȫ�����ڲ����-�۵Ĺ����У�����Һ��pHֵ��1������3.7��ʹFe3+ת�����������������Ҳ������������ʣ�����ѡ���������ȷ�ĩ��
�ʴ�Ϊ��B��E��
��3��������ϡ���ᣬ�����ᱵ���ɣ�����������⣬��Fe2+����ΪFe3+���ٵ�����ҺpH��ˮ�����������������������������������������Ҫ�ɷ���BaSO4��Fe��OH��3���ʴ�Ϊ��Fe��OH��3��BaSO4��
��4����ˮ�Ȼ��Ⱦ���61��ʱ��ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ�������ȷ紵����ˮ�Ȼ��ȣ�ѡ��������¶ȷ�Χ��50��60�棬
�ʴ�Ϊ��A��
��5�������ܽ�ƽ�⣬�Ҳ������������ʣ��������ѡ�õ���ϴ�Ӽ��ǣ������Ȼ�����Һ��
�ʴ�Ϊ�������Ȼ�����Һ��
���� ���⿼���Ʊ�ʵ�鷽������ƣ������Ʊ���������ԭ���ǽ��Ĺؼ����漰��Ӧ����Ӱ�����ء����ʵķ����ᴿ�����������Ŀ������Լ�ѡ��ȣ�ע�����Ŀ��Ϣ����ѧ֪ʶ���ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ�


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д� �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ڢ� | C�� | �ڢۢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ֱ��ȼ���к������ɵ��DZ� | |
| B�� | �ֱ������ˮ�����ú�ֲ㣬�ϡ����������ɫ����ʧ���Ǽ�ϩ | |
| C�� | �ֱ������ˮ�����ú�ֲ㣬�²����ɫ��ʧ���Ǽ�ϩ | |
| D�� | �ֱ�������Ը��������Һ�������ú�ˮ����ɫ��ʧ���Ǽ�ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
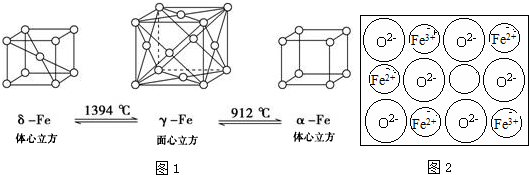
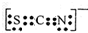 ��Fe3+��SCN-�����γ���λ��1��6�������ӣ���Fe3+��SCN-�Ը�����1��5��ϣ���FeCl3��KSCN��ˮ��Һ�з�����Ӧ�Ļ�ѧ����ʽ���Ա�ʾΪFeCl3+5KSCN=K2[Fe��SCN��5]+3KCl��
��Fe3+��SCN-�����γ���λ��1��6�������ӣ���Fe3+��SCN-�Ը�����1��5��ϣ���FeCl3��KSCN��ˮ��Һ�з�����Ӧ�Ļ�ѧ����ʽ���Ա�ʾΪFeCl3+5KSCN=K2[Fe��SCN��5]+3KCl���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��ˮ�������H+�������ڣ��� | |
| B�� | ����Һ�������ӵ���Ũ��С��0.01 mol•L-1 | |
| C�� | ����Һ�У�n��OH-��=n��HCO3-��+2n��H2CO3��+n��H+�� | |
| D�� | ����Һ�У�c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com